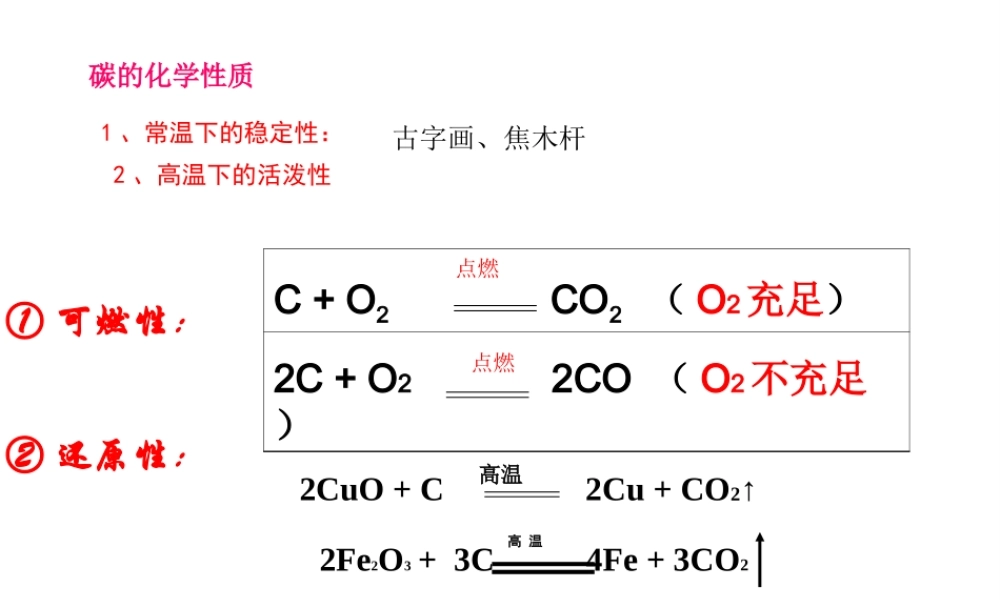
高温① 可燃性:2CuO + C 2Cu + CO2↑② 还原性:C + O2 CO2 ( O2 充足)2C + O2 2CO ( O2 不充足)点燃点燃2Fe2O3 + 3C 4Fe + 3CO2 高 温高 温 碳的化学性质1 、常温下的稳定性:2 、高温下的活泼性古字画、焦木杆C + CO2 2CO( 吸收热量 )发生发生装置装置药品反应原理收集装置验满方法温故知新——回忆氧气的实验室制法高锰酸钾或氯酸钾、二氧化锰过氧化氢溶液、二氧化锰2KMnO4 = K2MnO4 + MnO2 +O2↑2 KClO2 KClO33 = 2 KCl + 3 O = 2 KCl + 3 O2 2 ↑↑2H2O2 === 2H2O + O2↑将一根带火星的木条放在瓶口,若木条复燃,证明已满△MnO2△MnO2 实验室制取气体的一般思路确定制取气体的化学反应原理2
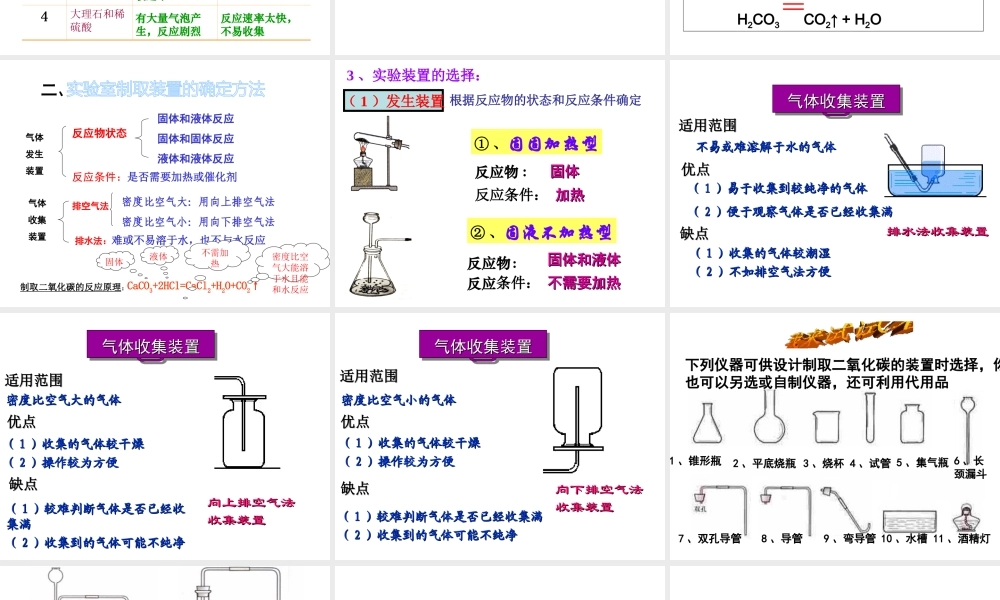
制取气体的实验装置 发生装置 收集装置3
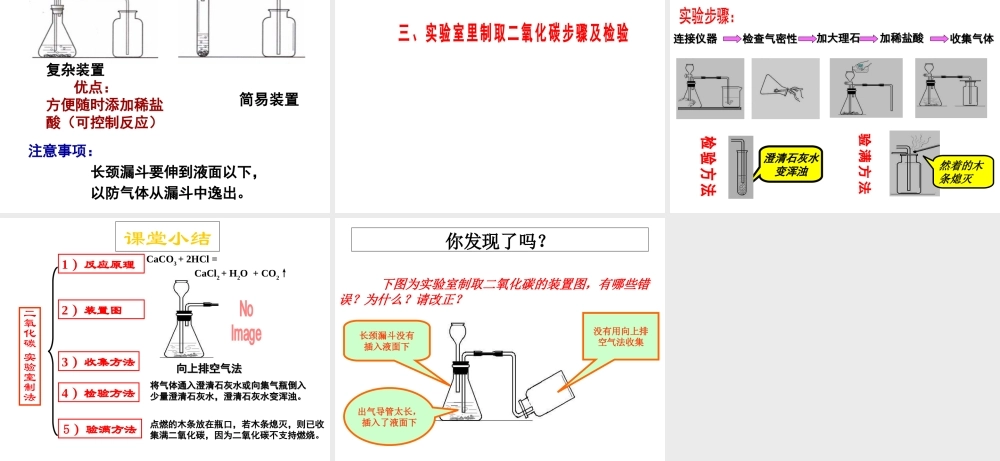
制取气体操作实验步骤验满1
三、探究选用的药品编号实验内容实验现象实验分析1Na2CO3 粉末和稀盐酸 2CaCO3 粉末和稀盐酸 3大理石和稀盐酸 4大理石和稀硫酸有大量气泡产生,反应剧烈 有大量气泡产生,反应剧烈 反应速率太快,不易收集 反应速率太快,不易收集 产生气泡速率比较适中 适合实验室制取二氧化碳气体有大量气泡产生,反应剧烈 反应速率太快,不易收集 • 注意:• 不用稀硫酸
因为硫酸与石灰石反应生成微溶于水的硫酸钙,覆盖在石灰石的表面,阻止石灰石与稀硫酸的反应
• 不用碳酸钠
因为碳酸钠与稀盐酸反应时速度过快,不容易控制反应过程,不利于收集气体
• 不用浓盐酸
因为浓盐酸有强挥发性,可挥发出氯化氢气体,使得到的二氧化碳不纯
一、实验室制取二氧化碳的反应原理大理石或石灰石跟稀盐酸反应制取二氧化碳气体 CaCO3 + 2HCl CaCl2 + CO2↑+H2O 这个反应分两步