第三单元 物质构成的奥秘 原子的结构原子原子核( + )核外电子 (-) 质子( +)中子每个质子带一个单位的正电荷不带电每个电子带一个单位的负电荷核电荷数=质子数=核外电子数(不显电性)【【相对原子质量相对原子质量】】以一种碳原子以一种碳原子 (( 其中含其中含 66 个质个质子和子和 66 个中子个中子 )) 质量的质量的 1/121/12 为标准,其他原子为标准,其他原子的质量跟它相比较所得的比值,作为这种原子的的质量跟它相比较所得的比值,作为这种原子的相对原子质量
(符号为相对原子质量
(符号为 AArr )) 相对原子质量相对原子质量 相对原子质量相对原子质量相对原子质量 = (AArr)某种原子的质量一种碳原子质量 ×1 / 12≈≈ 1
67×101
67×10-27-27KgKg标准标准==一个碳一个碳 1212 原子的质量原子的质量 111212×× ♣ Ar 只是比值,不是原子的实际质量 ♣ Ar 有单位,单位为“ 1” ,常省略 ♣ 1 个质子大约是 1 个电子质量的 l836 倍,所以原子的质量主要集中在原子核上 ♣ 相对原子质量≈质子数 + 中子数第一层第二层第三层钠原子的结构( 11 个电子)核外电子的运动有自己特点,它不像行星绕太阳旋转有固定的轨道,原子核外的电子能量不同,能量大的在离核较远的区域运动,能量较小的在离核较近的区域运动,科学家把这些区域称为电子层
核外电子是在不同的电子层内运动的,人们把这种现象叫做核外电子排布
解释:核外电子的分层排布 三
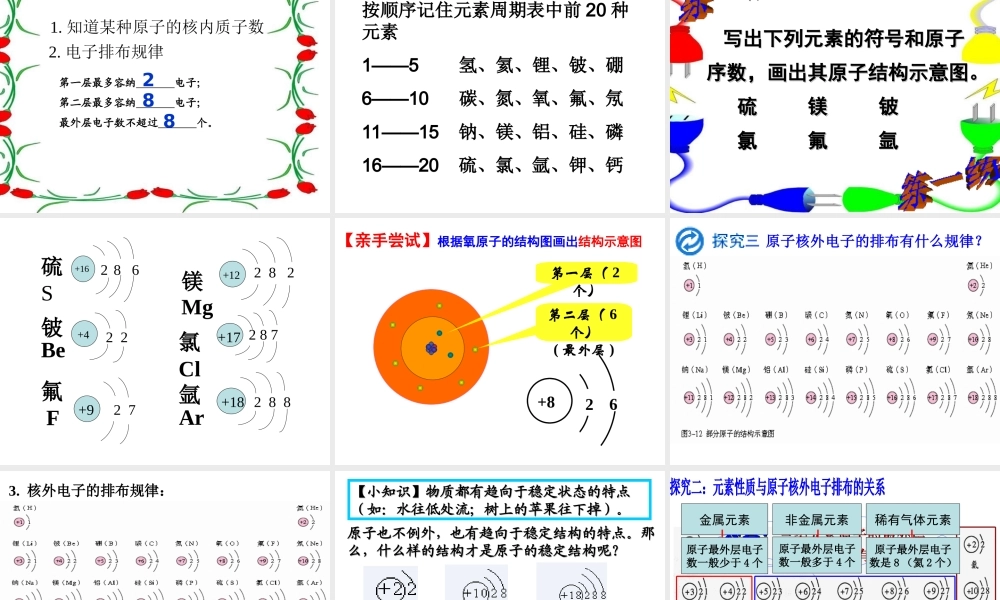
原子核外电子的排布 1
核外电子的分层排布1 2 3 4 5 6 7能量低的在离核近的区域运动,能量高的在离核远的区域运动
核外电子分层排布规律近 远低 高核外电子分层排布示意图电子层:离 核: 能 量: 第一层( 2个)第二层( 8个)第三层( 1 个)(最外层)钠原子的结构( 11