课时15专题提升(本课时对应学生用书第66~68页)【微专题】微小专题1常见物质的制备1
合金(1)概念:合金是指两种或两种以上的金属(或金属与非金属)熔合而成的具有金属特性的物质
(2)性能:合金具有不同于各成分金属的物理、化学性能或机械性能
①熔点:一般比它的各成分金属低
②硬度和强度:一般比它的各成分金属大
金属冶炼方法金属的活动性顺序KCaNaMgAlZnFeSnPb(H)CuHgAgPtAu金属原子失电子能力强→弱金属离子得电子能弱→强力主要冶炼方法电解法热还原法热分解法物理方法(1)电解法冶炼金属2Al2O3(熔融)4Al+3O2↑MgCl2(熔融)Mg+Cl2↑2NaCl(熔融)2Na+Cl2↑(2)热还原法①焦炭还原法,如C+2CuO2Cu+CO2↑②一氧化碳还原法,如3CO+Fe2O32Fe+3CO2③氢气还原法,如4H2+Fe3O43Fe+4H2O④活泼金属还原法,如2Al+Cr2O3Al2O3+2Cr、10Al+3V2O56V+5Al2O3(3)热分解法2HgO2Hg+O2↑2Ag2O4Ag+O2↑3
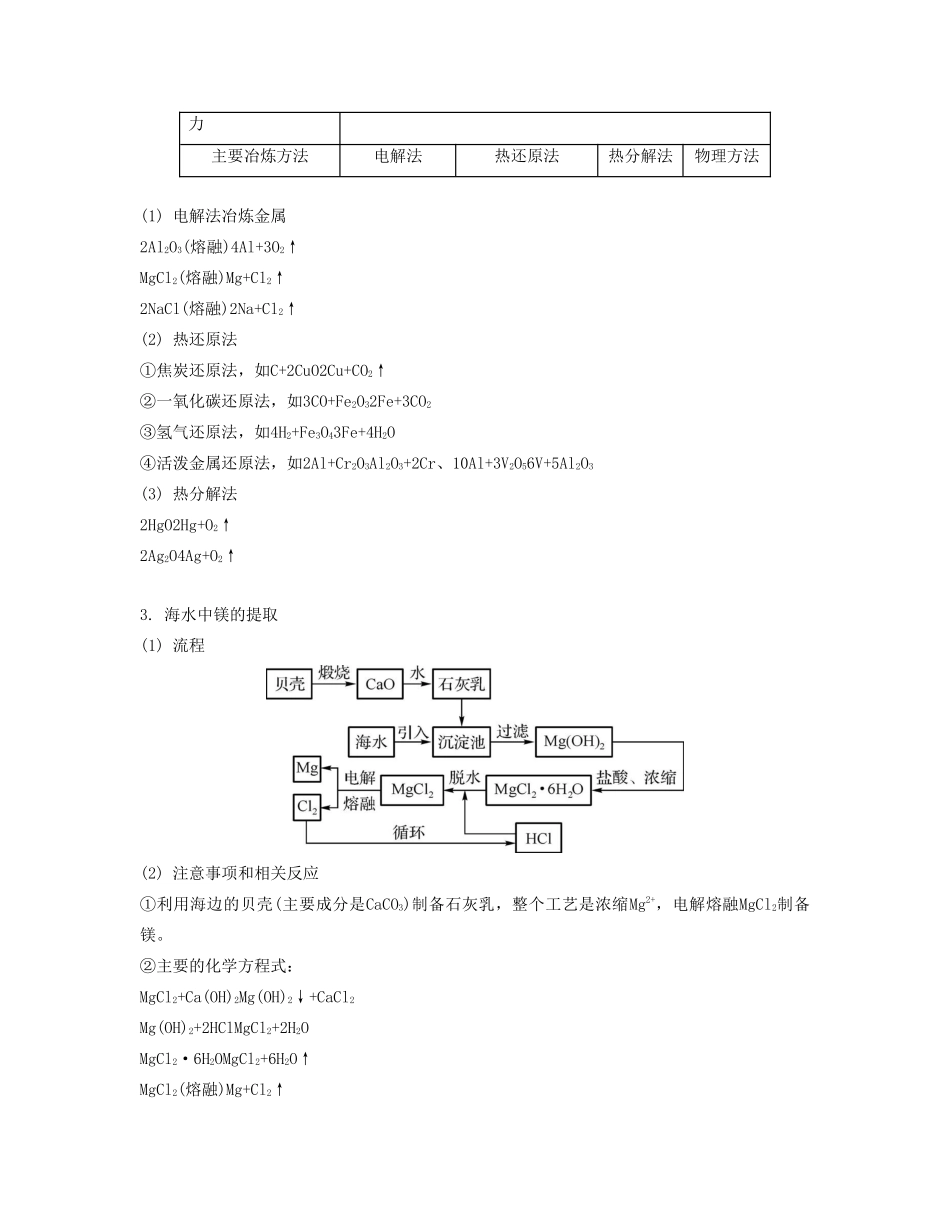
海水中镁的提取(1)流程(2)注意事项和相关反应①利用海边的贝壳(主要成分是CaCO3)制备石灰乳,整个工艺是浓缩Mg2+,电解熔融MgCl2制备镁
②主要的化学方程式:MgCl2+Ca(OH)2Mg(OH)2↓+CaCl2Mg(OH)2+2HClMgCl2+2H2OMgCl2·6H2OMgCl2+6H2O↑MgCl2(熔融)Mg+Cl2↑4
铝土矿(含Al2O3、Fe2O3等)炼铝(1)流程(2)注意事项和相关反应①溶解铝土矿的方法有酸溶法(H2SO4溶液)和碱溶法(NaOH溶液),该流程采用碱溶法
②主要的化学方程式:Al2O3+2NaOH2NaAlO2+H2ONaAlO2+2H2O+CO2Al(OH)3↓+NaHCO32Al(OH)3Al2O3