第四单元物质构成的奥秘课题1原子的构成教学目标1、解原子的组成,核电荷数、质子数和核外电子数的关系
2.了解相对原子质量的概念以及相对原子质量和原子组成的关系
3、会查相对原子质量表
重点难点原子和相对原子质量概念的形成
教学方法实验学习法、问题解决法、情境教学法、经验中学习、课堂讨论法
教学过程引入分子虽然很小,但却是真实存在的,而且在化学反应中具有可分性
那么,怎样证明分子的可分性呢
通过物质的分解反应可以从宏观上观察到一种物质分解生成两种或两种以上的其他物质
例:(大屏幕显示氧化汞受热分解的示意图,教师边操作边讲解)(学生讨论并回答)你观察到了什么现象
通过这些现象可得出什么结论
写出这个反应的文字表达式
(教师根据学生的回答讲解)氧化汞分子是由更小的微粒构成的,受热时氧化汞分子分解为汞原子和氧原子,许多汞原子聚集成金属汞,每两个氧原子结合成一个氧原子,许多氧原子聚集成氧气,可见,在化学反应中,氧化汞分子是可以再分的,而汞原子和氧原子是不能再分的
(板书)(教师启发式提问)在化学反应中原子的不能再分的,那么用其他方法能不能把原子再进行分割呢
今天我们就来探讨这个问题
(板书课题)原子的结构:1、(学生观察大屏幕上的结构示意图,分析原子的结构
)(教师适时的提示启发,引导学生充分利用大屏幕上的表格,分析原子各部分的带电情况
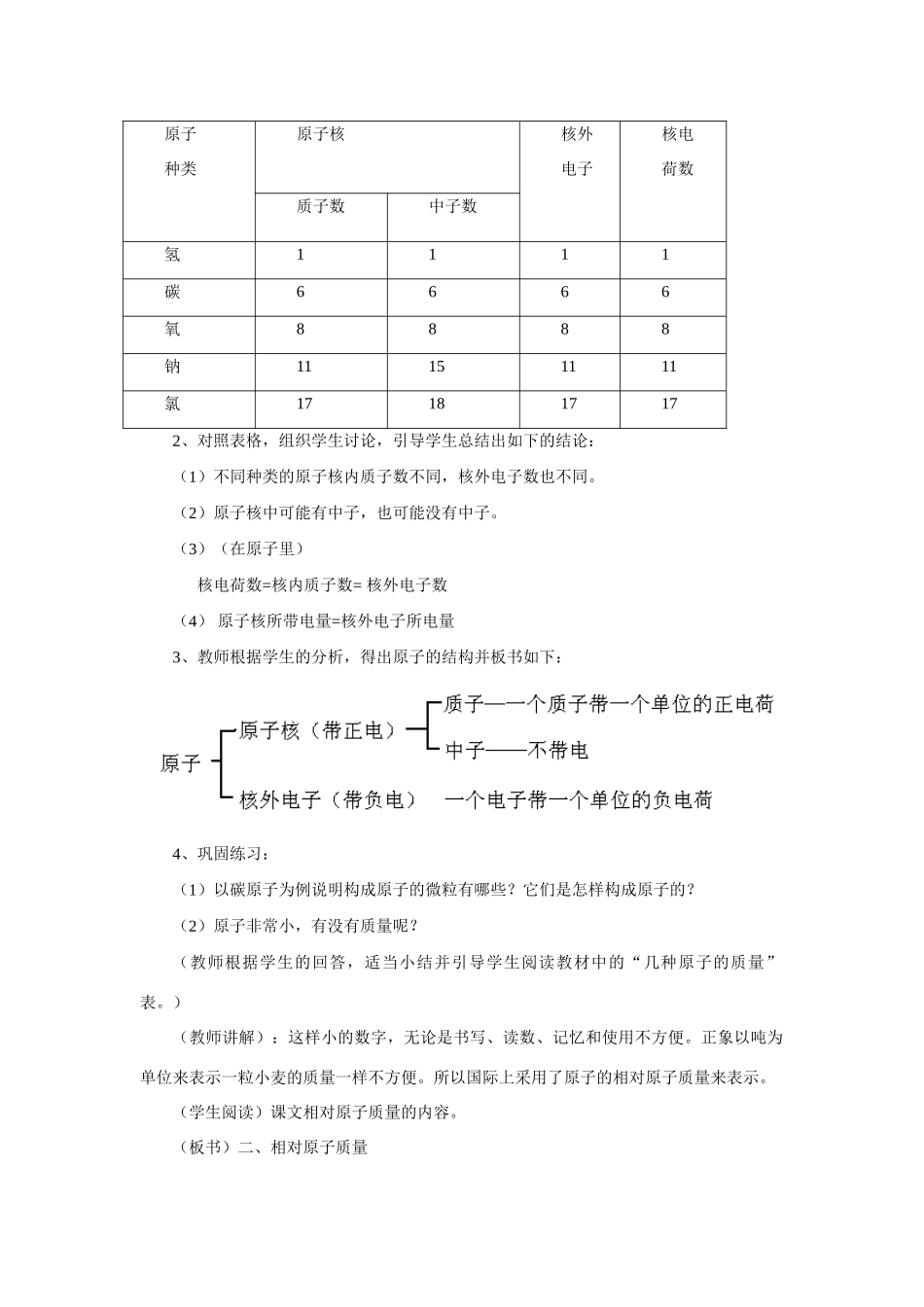
)附:表格原子种类原子核核外电子核电荷数质子数中子数氢1111碳6666氧8888钠11151111氯171817172、对照表格,组织学生讨论,引导学生总结出如下的结论:(1)不同种类的原子核内质子数不同,核外电子数也不同
(2)原子核中可能有中子,也可能没有中子
(3)(在原子里)核电荷数=核内质子数=核外电子数(4)原子核所带电量=核外电子所电量3、教师根据学生的分析,得出原子的结构并板书如下:4、巩固练习:(1)以碳原子为例说明构成原子的微粒