第二单元原电池化学电源一、单项选择题1.下列过程属于化学能转化为电能的是()A.行人踩踏发电瓷砖(原理是利用行人踩踏地板产生的振动来发电)B.智能手机电池放电C.汽车发电机中汽油燃烧D.氢氧化钠与盐酸反应解析:选B
A选项,动能转化为电能,错误;B选项,化学能转化为电能,正确;C选项,化学能转化为动能,错误;D选项,化学能转化为热能,错误
2.下列电池工作时,O2在正极放电的是()A
氢燃料电池C
镍镉电池解析:选B
锌锰电池,正极反应:MnO2+H2O+e-===MnOOH+OH-,MnO2在正极放电,A错误
氢燃料电池,正极反应(酸性条件下):O2+4H++4e-===2H2O,O2在正极放电,B正确
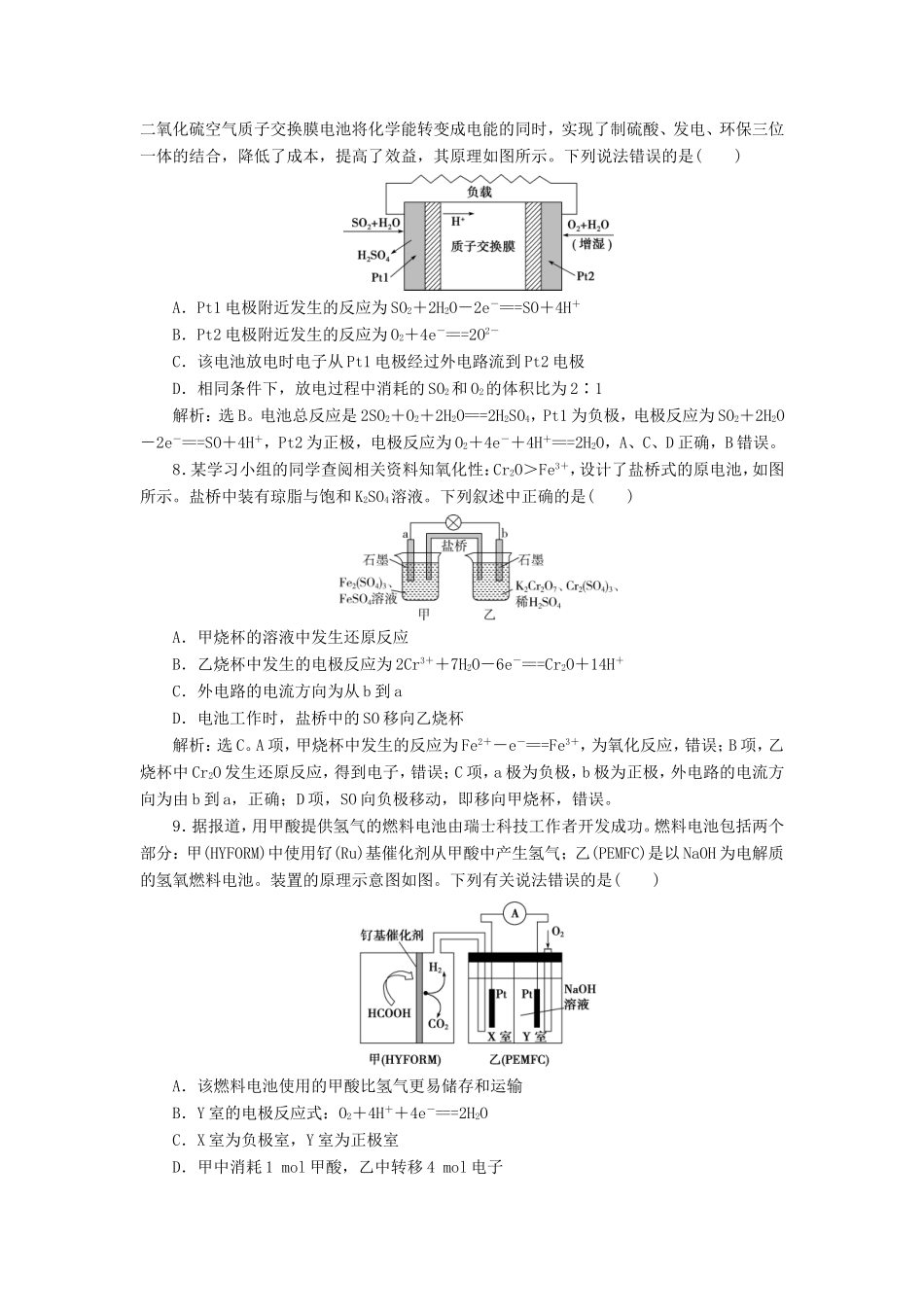
铅蓄电池,正极反应:PbO2+4H++SO+2e-===PbSO4+2H2O,PbO2在正极放电,C错误
镍镉电池,正极反应:NiOOH+H2O+e-===Ni(OH)2+OH-,NiOOH在正极放电,D错误
3.图1是铜锌原电池示意图
图2中,x轴表示实验时流入正极的电子的物质的量,y轴表示()A.铜棒的质量B.c(Zn2+)C.c(H+)D.c(SO)解析:选C
该装置构成原电池,Zn是负极,Cu是正极
在正极Cu上溶液中的H+获得电子变为氢气,Cu棒的质量不变,错误;B
由于Zn是负极,不断发生反应Zn-2e-===Zn2+,所以溶液中c(Zn2+)逐渐增大,错误;C
由于反应不断消耗H+,所以溶液中c(H+)逐渐减小,正确;D
SO不参加反应,其浓度不变,错误
4.(2020·广州模拟)某小组为研究原电池原理,设计如图装置,下列叙述正确的是()A.若X为Fe,Y为Cu,则铁为正极B.若X为Fe,Y为Cu,则电子由铜片流向铁片C.若X为Fe,Y为C,则碳棒上有红色固体析出D.若X为Cu,Y为Zn,则锌片发生还原反应解析:选C
Fe比Cu活