第一章化学反应与能量第一节化学反应与能量的变化[阅读提纲]1
什么是反应热(焓变)
什么是放热反应和吸热反应
什么是热化学方程式
在热化学方程式中如何表示放热和吸热
为什么在热化学方程式中必须标明物质的集聚状态
热化学方程式中的系数表示什么
能否用分数表示
一.反应热焓变1.定义:化学反应过程中所释放或吸收的能量都属于反应热,又称为焓变(ΔH),单位kJ/mol
化学反应中为什么会伴随能量变化
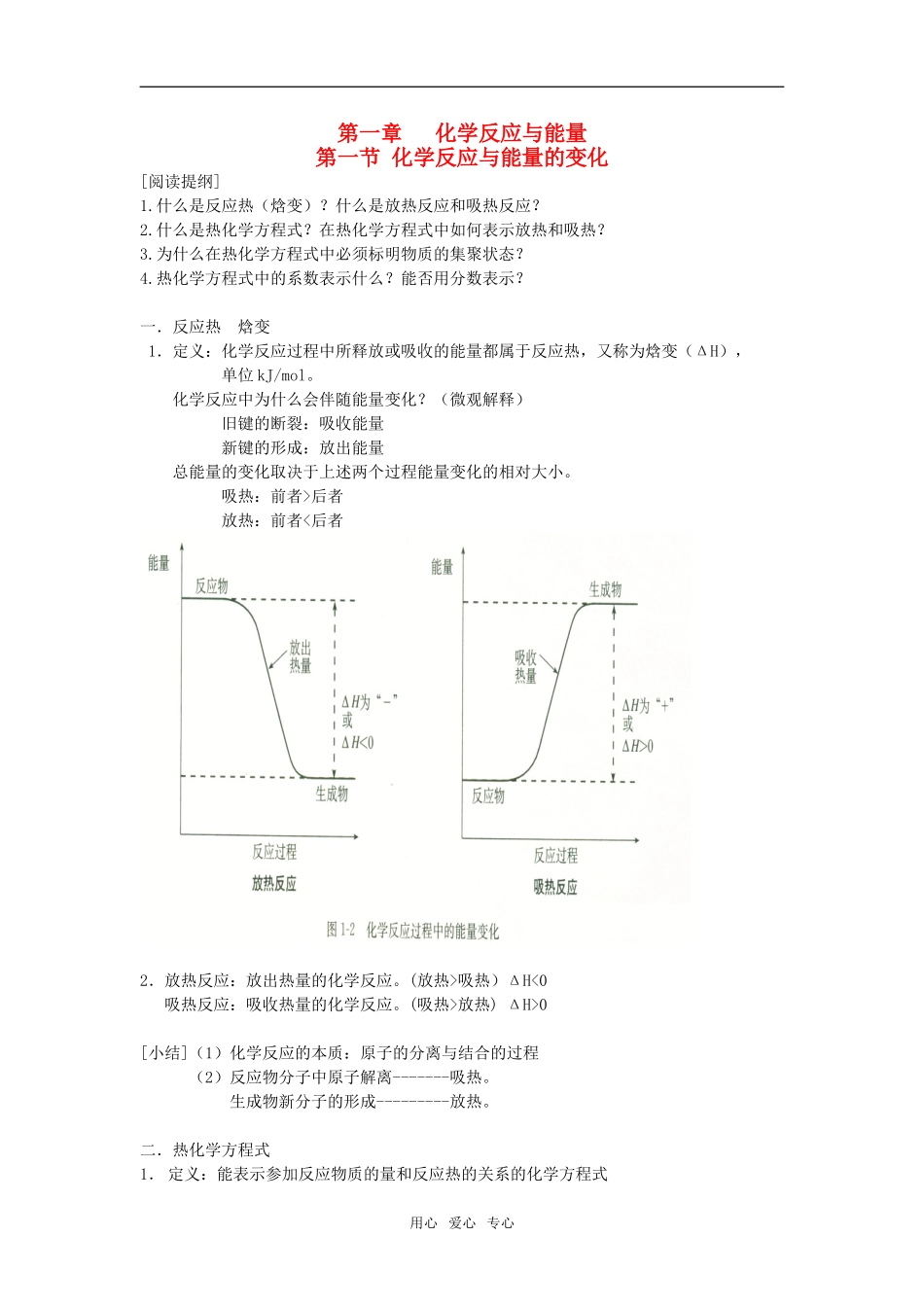
(微观解释)旧键的断裂:吸收能量新键的形成:放出能量总能量的变化取决于上述两个过程能量变化的相对大小
吸热:前者>后者放热:前者吸热)ΔH放热)ΔH>0[小结](1)化学反应的本质:原子的分离与结合的过程(2)反应物分子中原子解离-------吸热
生成物新分子的形成---------放热
二.热化学方程式1.定义:能表示参加反应物质的量和反应热的关系的化学方程式用心爱心专心例如:H2(气)+1/2O2(气)=H2O(气)ΔH=-241
8kJ/molH2(气)+1/2O2(气)=H2O(液)ΔH=-285
8kJ/mol[讨论]1
为什么集聚状态不同,热量值不同
答:液态水变成水蒸气要吸收热量2
若反应物状态不同,而生成物状态相同,那么热量值相同吗
答:不同[思考与交流]2.书写要点:C(固)+H2O(气)=CO(气)+H2(气)ΔH=+131
3kJ/mol①标集聚状态(固、液、气)②右端标热量数值和符号:吸热用“+”,放热用:“-”
③系数单位是“摩”,而不是“个”;也不能表示物质的量之比
④系数可用分数,但热量值要相应变化
如:2H2(气)+O2(气)=2H2O(液)ΔH=-571
6kJ/molH2(气)+1/2O2(气)=H2O(液)ΔH=-285
8kJ/mol⑤不注明条件,即指250C、1
01×105Pa例:1克甲烷在空气中燃烧,恢复常温下测得放出热量5