原子核外电子排布所遵循的原理原子轨道[明确学习目标]1
了解能量最低原理,知道基态与激发态及原子核外电子在一定条件下会发生跃迁产生原子光谱
了解原子核外电子的运动状态;知道电子云和原子轨道;掌握泡利原理和洪特规则;掌握1~36号元素的原子核外电子排布式和电子排布图
学生自主学习一、能量最低原理、基态与激发态1.能量最低原理原子的电子排布遵循□构造原理能使整个原子的能量处于□最低状态
2.基态与激发态基态原子:处于□最低能量的原子叫做基态原子
激发态原子:基态原子的电子□吸收能量后,电子会跃迁到□较高能级,变为激发态原子
电子从□较高能量的激发态跃迁到□较低能量的激发态乃至基态时,将□释放能量
基态原子((((激发态原子
3.原子光谱不同元素的原子发生跃迁时会吸收或释放不同的光,可以用光谱仪摄取各种元素的电子的□吸收光谱或□发射光谱,总称原子光谱
二、电子云和原子轨道1.电子云(1)电子云是处于□一定空间运动状态的电子在原子核外空间的概率密度分布的形象化描述
(2)电子云轮廓图①将电子在原子核外空间出现的概率□P=90%的空间圈出来,制作电子云的轮廓图,便可描绘电子云的形状
②s电子、p电子的电子云轮廓图所有原子的任一能层的s电子的电子云轮廓图都是□球形的,同一原子的能层□越高,s电子云的半径□越大,如下图Ⅰ所示
这是由于1s、2s、3s……电子的能量依次增高,电子在离核更远的区域出现的概率逐渐□增大,电子云越来越向更大的空间扩展
除s电子云外,其他空间运动状态的电子云都不是球形的,如p电子云是□哑铃状的
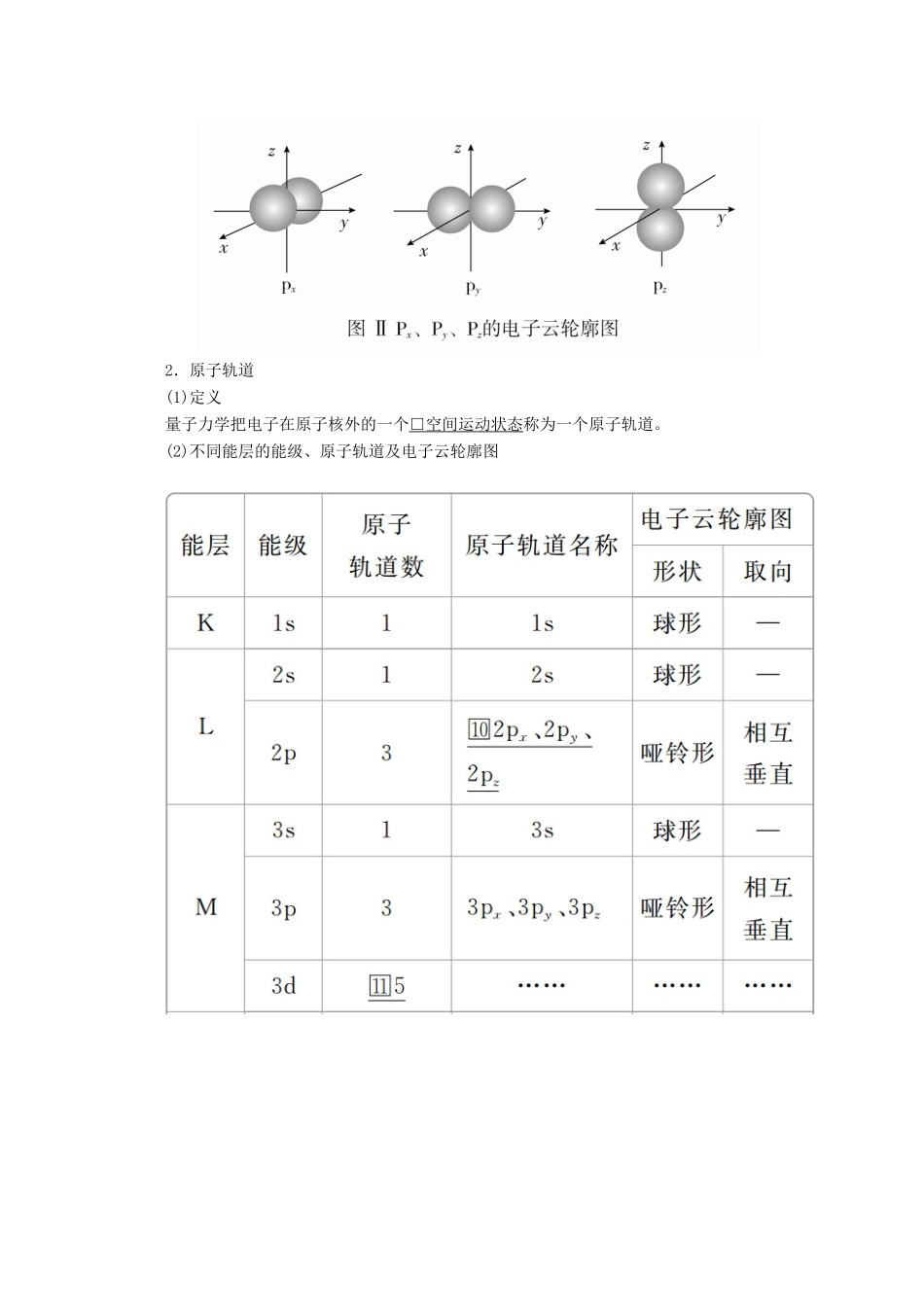
每个p能级都有3个□相互垂直的电子云,分别称为px、py和pz,如图Ⅱ所示
p电子云的平均半径随能层序数的增大而增大
2.原子轨道(1)定义量子力学把电子在原子核外的一个□空间运动状态称为一个原子轨道
(2)不同能层的能级、原子轨道及电子云轮廓图注:d轨道和f轨道各有名