第四节难溶电解质的溶解平衡[明确学习目标]1
了解难溶电解质的沉淀溶解平衡
了解沉淀转化的本质
学会用沉淀溶解平衡理论解决生产、生活中的实际问题
一、沉淀溶解平衡1.25℃时,溶解性与溶解度的关系2.沉淀溶解平衡(1)概念:在一定温度下,当沉淀□溶解的速率和沉淀□形成的速率相等时,即达到溶解平衡
(2)图示(3)表示方法:以AgCl为例,溶解平衡可表示为□AgCl(s)Ag+(aq)+Cl-(aq)
(4)特征二、沉淀反应的应用1.沉淀的生成(1)沉淀生成的应用在涉及无机制备、提纯、废水处理等领域,常利用生成沉淀来达到□分离或□除去某些离子的目的
(2)沉淀生成的方法①调节pH法:如工业原料氯化铵中含杂质氯化铁,使其溶解于水,再加入□氨水调节pH至7~8,可使Fe3+转变为□Fe(OH)3沉淀而除去
②加沉淀剂法:如以Na2S、H2S等作沉淀剂,使某些金属离子如Cu2+、Hg2+等生成极难溶的硫化物□CuS、□HgS等沉淀,是除去杂质常用的方法
其离子反应如下:Cu2++S2-===□CuS↓Cu2++H2S===□CuS↓+2H+Hg2++S2-===□HgS↓Hg2++H2S===□HgS↓+2H+2.沉淀的溶解(1)沉淀溶解的原理根据□平衡移动原理,对于在水中难溶的电解质,如果能设法不断地移去溶解平衡体系中的相应离子,使平衡向□沉淀溶解的方向移动,就可以使沉淀□溶解
(2)溶解方法①酸溶解法:利用较□强的酸溶解较弱酸的难溶盐
如CaCO3难溶于水,却易溶于盐酸,过程可表示为CaCO3(s)Ca2+(aq)+CO(aq),CO+H+□HCO,HCO+H+□H2CO3,H2CO3===□H2O+CO2↑
随着CO浓度的减少,沉淀溶解平衡不断右移,CaCO3逐渐溶解
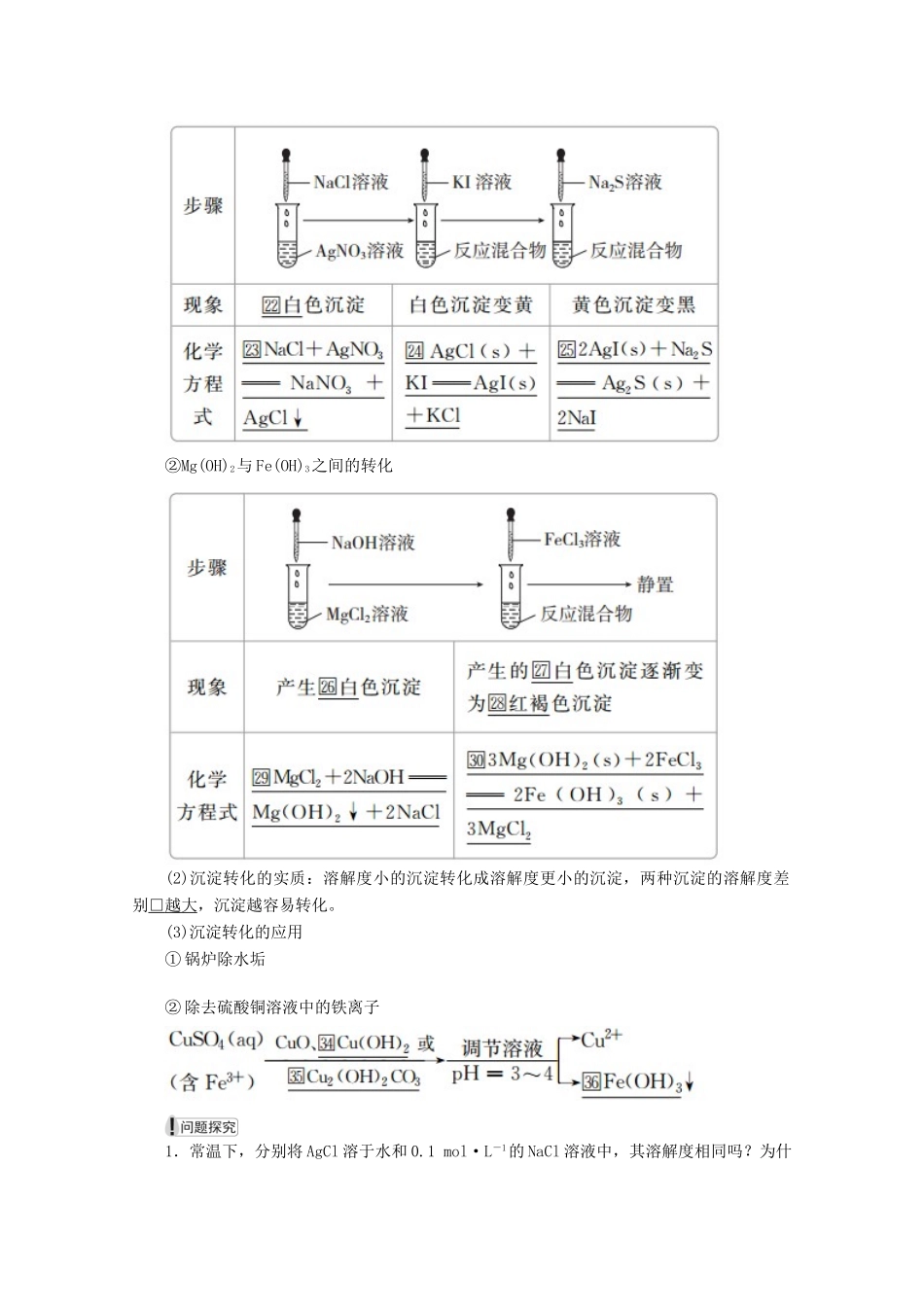
②盐溶液溶解法:3.沉淀的转化(1)沉淀转化实验①难溶性银盐之间的转化②Mg(O