10.1测定1mol气体的体积(共3+1课时)第1课时测定1mol气体体积的方法[设计思想]测定1摩尔气体体积的定量实验是教材的重点,也是学生学习的难点
它是帮助学生体会定性实验与定量实验区别,认识定量实验设计的方法,形成严谨思维品质和科学素养的重要载体
教学设计着重于学生自己对实验的设计、改进、完善
通过测定1摩尔气体体积的实验方案讨论与设计,了解定量实验设计的关键,概括出定量实验的基本原理与一般方法,掌握从具体到抽象的思维方法,以及间接测定的方法,体验定量测定中转化的思想方法对人类科学活动的影响与作用,初步形成严谨的科学态度和习惯
一.教学目标1.知识与技能(1)气体摩尔体积与温度和压强的关系(B)
(2)定性实验与定量实验的区别,定量实验中的直接测量与间接测量及其相互关系(A)
(3)测定1摩尔气体体积的实验设计技能(B)
2.过程与方法(1)综合已学过的知识,通过类比、迁移、分析,明白实验原理
(2)通过测定1摩尔气体体积的实验设计,认识定量测定中转化的思想方法
(3)初步学会间接测定的方法,提高分析、转化、归纳、总结的能力
3.情感态度与价值观通过测定1摩尔气体体积的实验设计,体验定量测定中转化的思想方法对人类科学活动的影响与作用,初步形成严谨的科学态度和习惯
二.教学重点和难点1.教学重点定量实验中直接测量与间接测量及相互关系2.教学难点探究设计测定1摩尔气体体积的实验方案三.教学用品药品:Mg、稀H2SO4、H2O仪器:媒体:电脑、投影仪四.教学流程1.流程图2.流程图说明引入:本章我们将学习几种定量测定方法
定量测定要求更理性、更科学,结果更精确,对现代化学的发展与进步有着不可替代的作用
下面我们首先学习测定1摩尔气体体积的方法
学生交流:决定物质所占体积大小有那些因素
1mol不同的固态和液态物质为什么其体积各不相同
影响气体体积的因素有那些
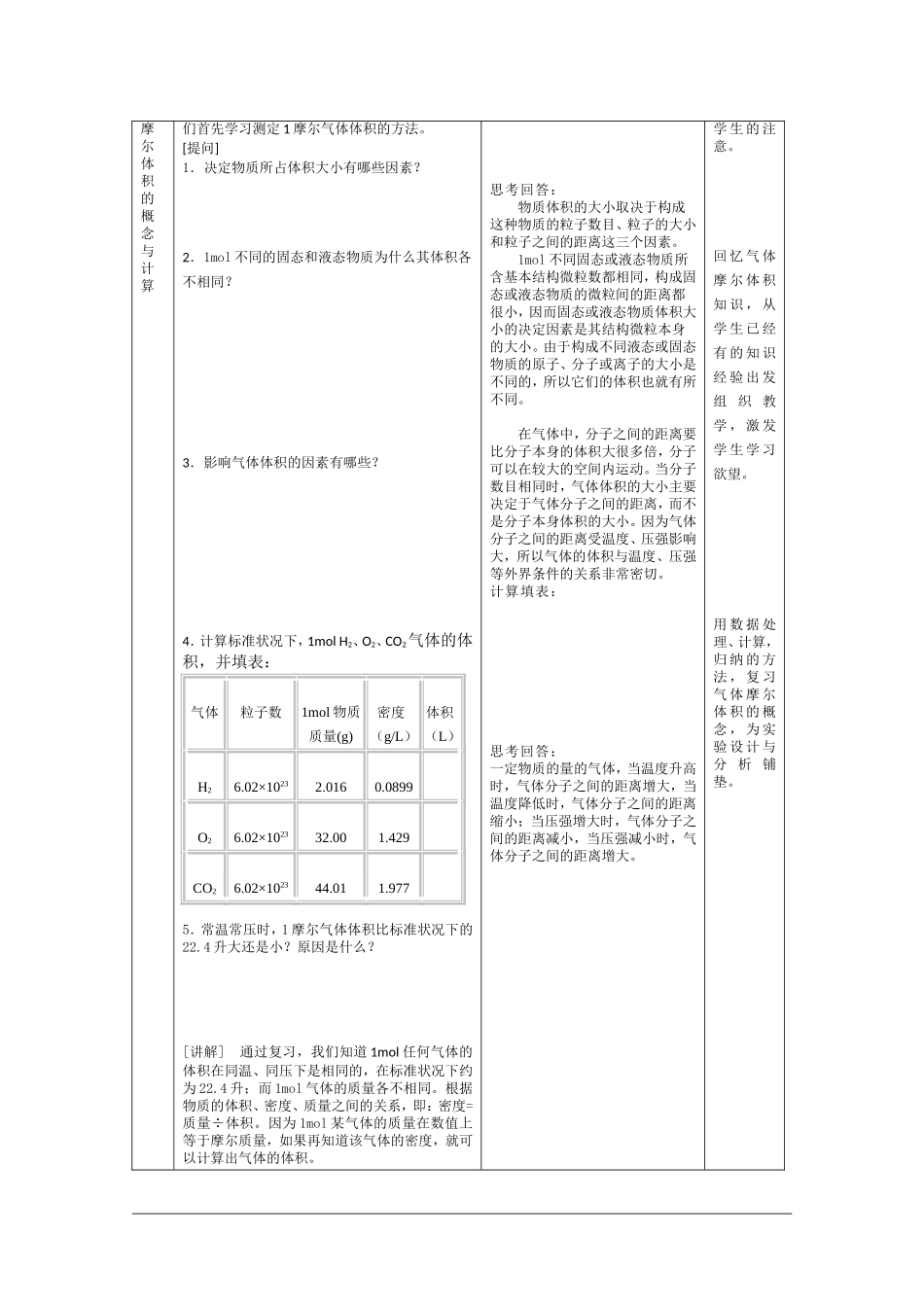
4.计算标准