元素周期律【教学目标】理解元素周期律【教学重点】元素性质的周期性变化【教学过程】〖引入〗元素周期表看起来很有规律,这个表的确是按一定的规律来排的,这个规律就是元素周期律
〖思考〗质子数和核电荷数有何关系
什么叫原子序数,应如何理解
[讨论]1、能否说:“质子数即核电荷数,也就是原子序数
”2、观察1—18号元素的原子结构示意图,研究以怎样的排列方式能使其有明显的规律性
这种规律是什么
3、原子序数的递增:(1)原子半径;(2)元素的金属性和非金属性强弱有何规律性变化
4、原子结构的角度来解释元素周期律的实质是什么
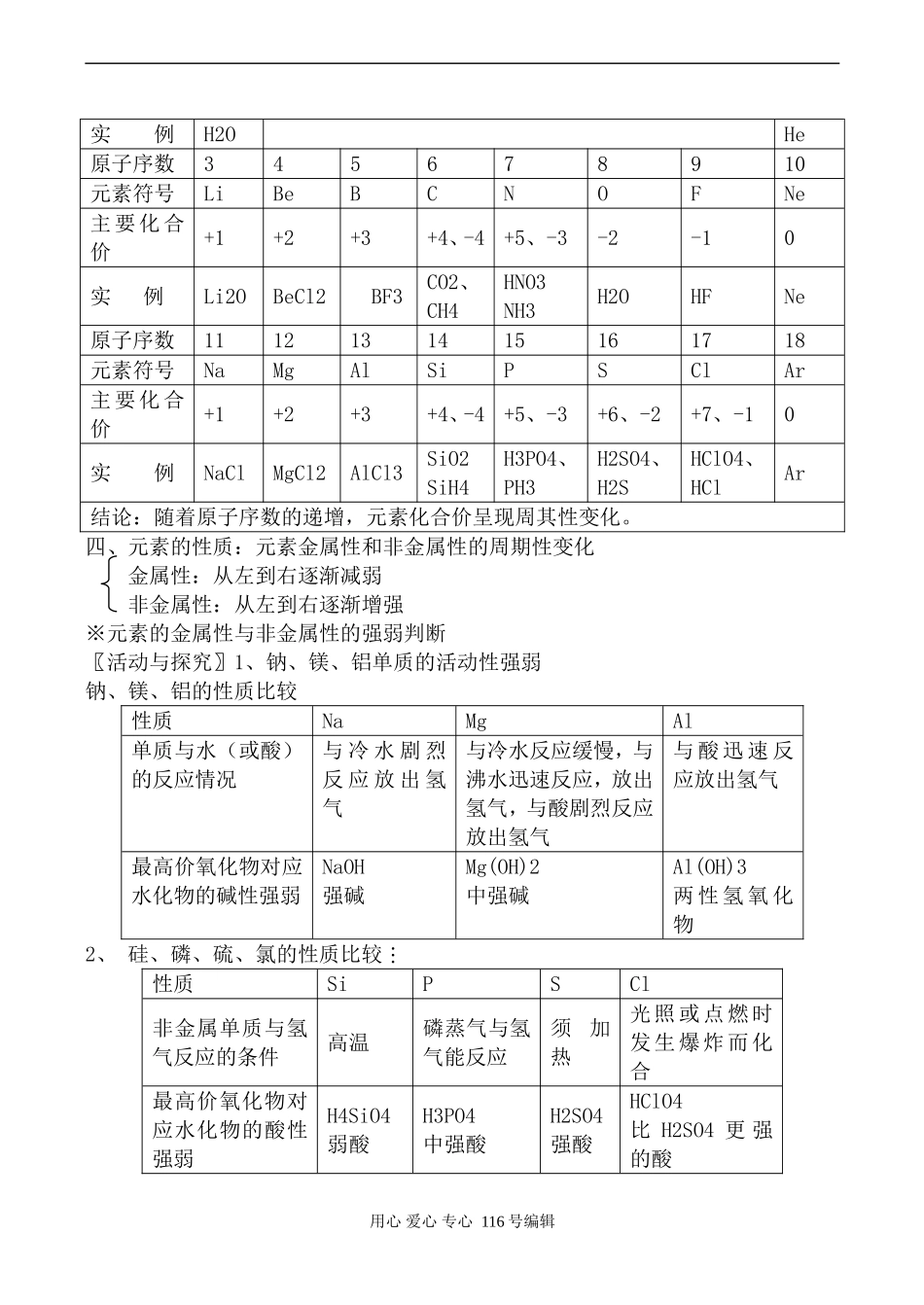
一、核外电子排布的周期性变化——最外层电子数由1-8周期性变化由1~18号元素原子结构示意图:原子序数电子层数最外层电子数达到稳定结构时的最外层电子数1~211~223~1021~8811~1831~88结论:随着原子序数的递增,元素原子的最外层电子排布呈现——变化
二、原子半径的周期性变化——从左到右半径缩小(稀有气体突大)随着原子序数的递增,元素原子半径变化的规律性原子序数原子半径的变化3~9大→小11~17大→小结论:随着原子序数的递增,元素原子半径呈现周期性的变化
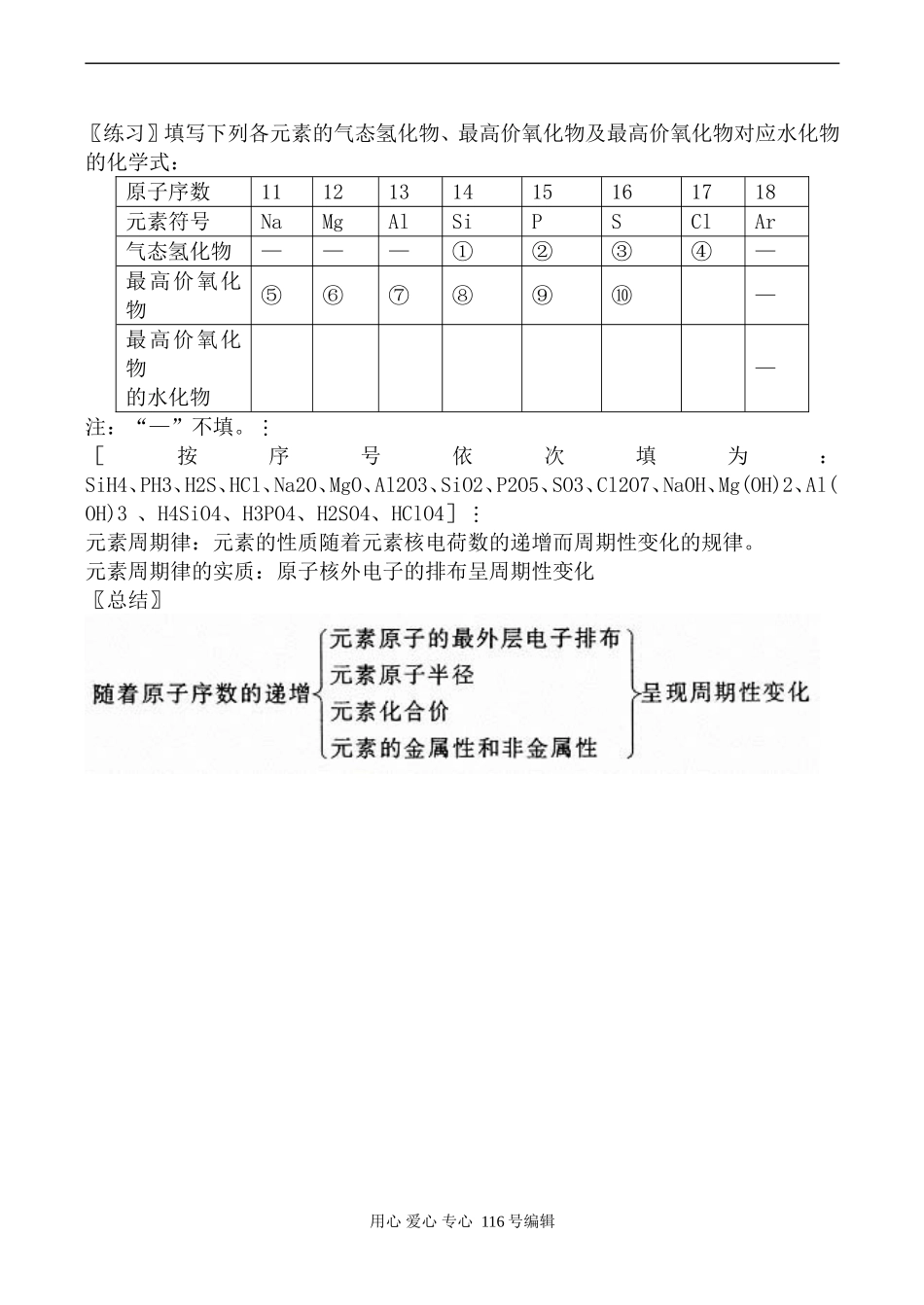
三、元素的化合价最高正价:+1+7负价:-4-1元素的主要化合价及实例原子序数12元素符号HHe主要化合价+1O用心爱心专心116号编辑实例H2OHe原子序数345678910元素符号LiBeBCNOFNe主要化合价+1+2+3+4、-4+5、-3-2-10实例Li2OBeCl2BF3CO2、CH4HNO3NH3H2OHFNe原子序数1112131415161718元素符号NaMgAlSiPSClAr主要化合价+1+2+3+4、-4+5、-3+6、-2+7、-10实例NaClMgCl2AlCl3SiO2SiH4H3PO4、PH3H2SO4、H2SHClO4、HClAr结论:随着原子序数的