第二节元素周期律(第三课时)【学习目标】(1)、掌握元素周期表和元素周期律的应用
(2)、了解周期表中金属元素、非金属元素分区
(3)、掌握元素化合价与元素在周期表中的位置关系
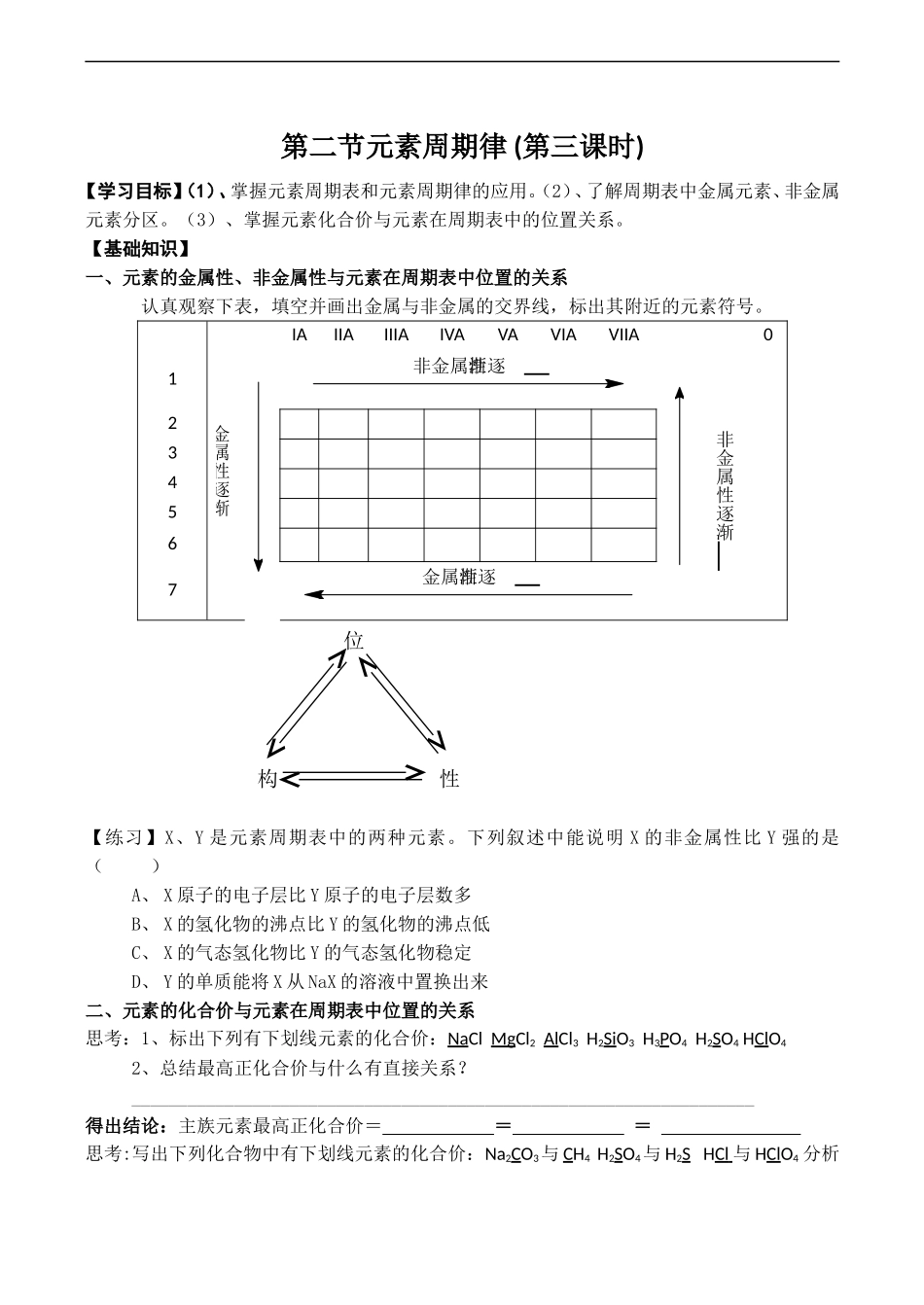
【基础知识】一、元素的金属性、非金属性与元素在周期表中位置的关系认真观察下表,填空并画出金属与非金属的交界线,标出其附近的元素符号
金属性逐渐IAIIAIIIAIVAVAVIAVIIA01非金属性逐渐非金属性逐渐234567金属性逐渐【练习】X、Y是元素周期表中的两种元素
下列叙述中能说明X的非金属性比Y强的是()A、X原子的电子层比Y原子的电子层数多B、X的氢化物的沸点比Y的氢化物的沸点低C、X的气态氢化物比Y的气态氢化物稳定D、Y的单质能将X从NaX的溶液中置换出来二、元素的化合价与元素在周期表中位置的关系思考:1、标出下列有下划线元素的化合价:NaClMgCl2AlCl3H2SiO3H3PO4H2SO4HClO42、总结最高正化合价与什么有直接关系
___________________________________________________________________得出结论:主族元素最高正化合价===思考:写出下列化合物中有下划线元素的化合价:Na2CO3与CH4H2SO4与H2SHCl与HClO4分析位构性最高正化合价与最低负化合价之间的关系,并解释其原因
【练习】某元素X的最高价氧化物对应水化物的化学式为HXO4,则其气态氢化物的化学式为:;若其水溶液呈现酸性,且能与AgNO3溶液反应生成白色沉淀,则它在元素周期表中的位置是:
三、元素周期律、元素周期表的应用1、预测未知物的位置与性质【练习】Ra(镭)是原子序数最大的第ⅡA族元素,下列说法不正确的是()A、原子半径是第ⅡA族中最大的B、遇冷水能剧烈反应C、位于第七周期D、Ra(OH)2是两性氢氧化物2、寻找所需