第2课时硫酸和硫酸根离子的检验一、硫酸1
硫酸的工业制法接触法制硫酸分为三个阶段,填写下表:三阶段三原料三反应(均放热)1
造气(生成SO2)2
接触氧化(生成SO3)3
SO3吸收(生成H2SO4)注意工业上制取硫酸常用浓硫酸而不用水吸收SO3,原因是SO3与水反应放热,易产生酸雾,影响SO3的吸收
硫酸的性质(1)物理性质纯净的硫酸是黏稠状液体,密度比水,能与水以任意比混合,沸点,难挥发
(2)酸的通性H2SO4在水里很容易电离出,具有,能使紫色石蕊溶液显,请写出下列反应的离子方程式
①和活泼金属(如Fe):;②和金属氧化物(如MgO):;③和碱[如Mg(OH)2]:;④和盐(如Na2CO3):
浓硫酸的特性实验室常用的浓硫酸质量分数为98
3%,密度为1
84g·cm3,比水,且浓度越大密度越大
沸点,挥发,常温下比较稳定
浓硫酸的三大特性:、和
(1)吸水性浓硫酸能够吸收气体、液体中的水分子及固体中的结晶水,故常用作
(2)脱水性-浓硫酸能把有机物中的氢和氧按脱去
如向蔗糖中加入浓硫酸时,蔗糖逐渐变黑,体积膨胀,形第1页共9页成固体,并放出有气味的气体
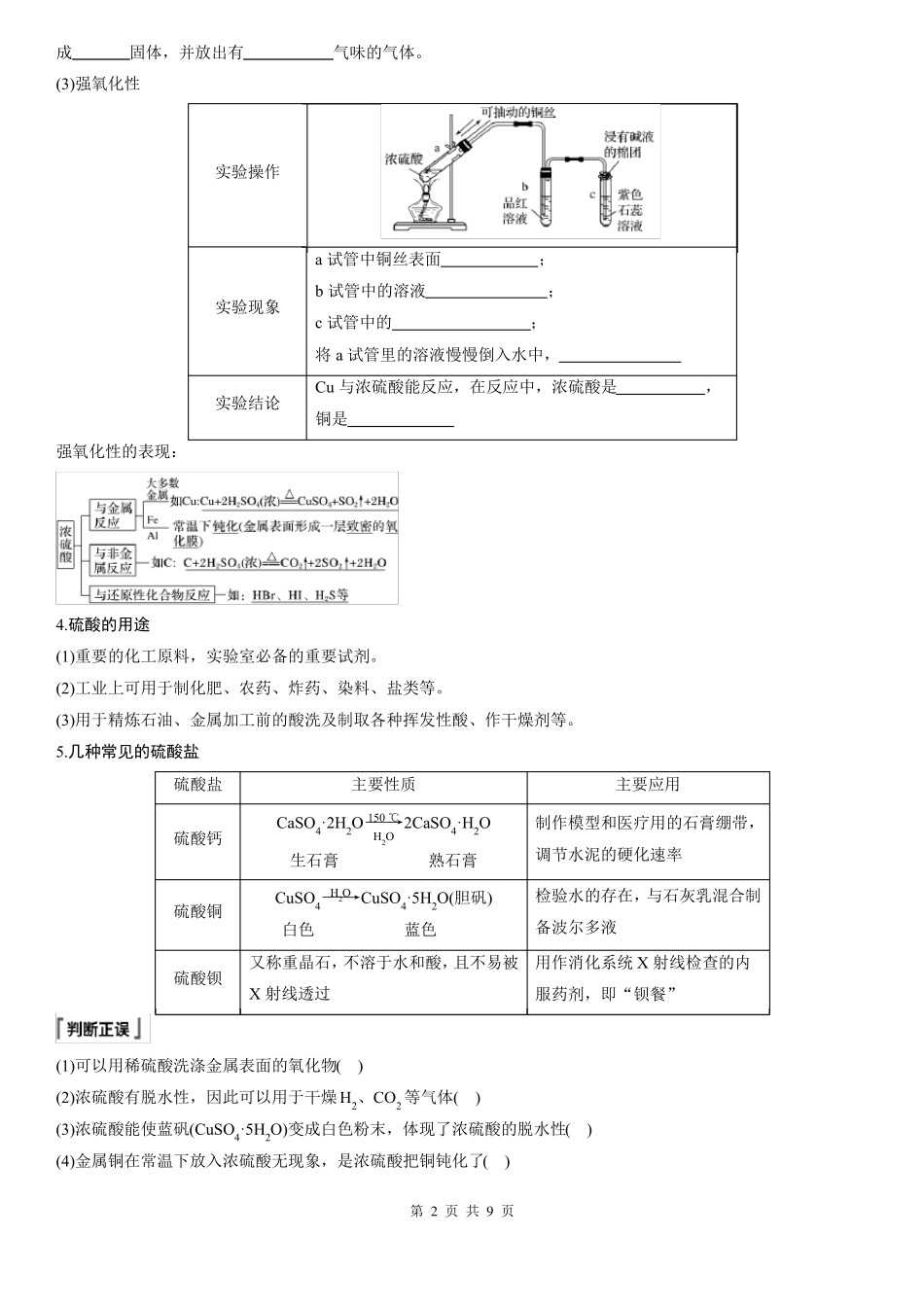
(3)强氧化性实验操作a试管中铜丝表面;实验现象b试管中的溶液;c试管中的;将a试管里的溶液慢慢倒入水中,实验结论强氧化性的表现:Cu与浓硫酸能反应,在反应中,浓硫酸是,铜是4
硫酸的用途(1)重要的化工原料,实验室必备的重要试剂
(2)工业上可用于制化肥、农药、炸药、染料、盐类等
(3)用于精炼石油、金属加工前的酸洗及制取各种挥发性酸、作干燥剂等
几种常见的硫酸盐硫酸盐硫酸钙主要性质CaSO4·2H2O――→2CaSO4·H2OHO2主要应用制作模型和医疗用的石膏绷带,调节水泥的硬化速率检验水的存在,与石灰乳混合制备波尔多液用作消化系统X射线检查的内服药剂,即“钡餐”150℃生石膏熟石膏硫酸铜CuSO4