突破点3离子反应提炼1离子共存与离子推断1
离子反应类型离子间通常能发生四种类型的反应,可以相互反应的离子不能大量共存
2“”.离子共存中的四大题设陷阱条件类型常见表述误点点拨常见的限制条件“”无色Cu2+、Fe2+、Fe3+、MnO等有色离子不能大量存在“pH=1”“或pH=13”溶液显酸性或碱性“因发生氧化还原反应而不只能是氧化性离子和还原性离子不共”能共存存,并不是其他离子反应,同时要注意溶液酸碱性的影响常见的易错点“”透明“”“”透明也可有色“”不能共存“”易错看成能共存常见的隐含条件“与Al反应放出H2”溶液既可能显酸性也可能显碱性“由水电离出c(H+)=1×10-12mol·L-1”的溶液溶液既可能显酸性也可能显碱性“通入足量的NH3”与NH3·H2O反应的离子不能存在常见题干要求(1)“”一定大量共存(2)“”可能大量共存(3)“”不能大量共存审清关键字词3
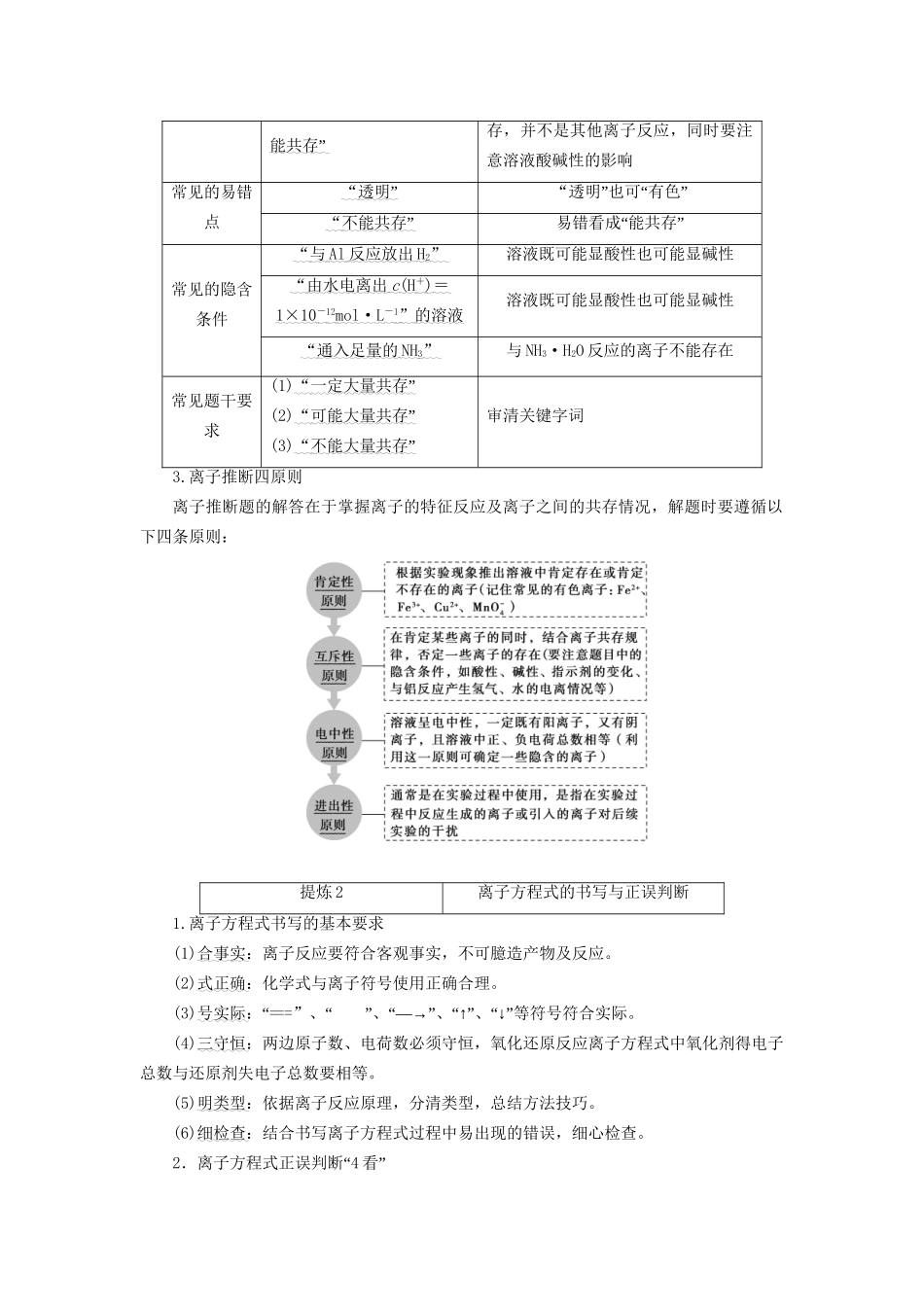
离子推断四原则离子推断题的解答在于掌握离子的特征反应及离子之间的共存情况,解题时要遵循以下四条原则:提炼2离子方程式的书写与正误判断1
离子方程式书写的基本要求(1)合事实:离子反应要符合客观事实,不可臆造产物及反应
(2)式正确:化学式与离子符号使用正确合理
(3)号实际“:===”“、”“、―→”“↑”“↓”、、等符号符合实际
(4)三守恒:两边原子数、电荷数必须守恒,氧化还原反应离子方程式中氧化剂得电子总数与还原剂失电子总数要相等
(5)明类型:依据离子反应原理,分清类型,总结方法技巧
(6)细检查:结合书写离子方程式过程中易出现的错误,细心检查
2“.离子方程式正误判断4”看(1)看拆分
易溶于水,易电离的强电解质用实际参加反应的离子表示;非电解质、弱电解质(弱酸、弱碱、水等),难溶物、气体、氧化物、单质等均用化学式表示
(2)看反应
检查离子方程式中各项是否都有公约数,检查是否漏写某个反应或