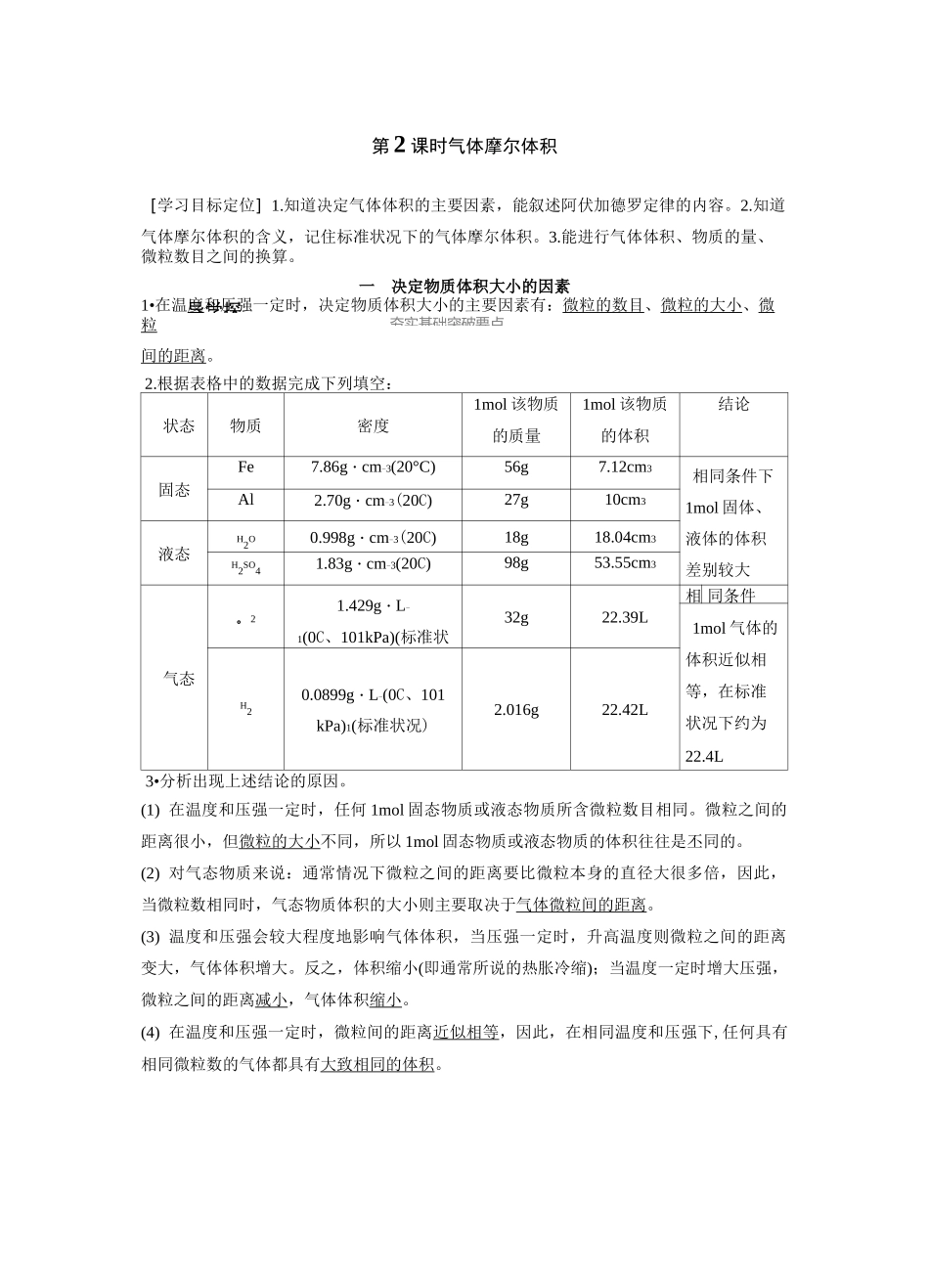
导学探夯实基础突破要点第2课时气体摩尔体积[学习目标定位]1.知道决定气体体积的主要因素,能叙述阿伏加德罗定律的内容。2.知道气体摩尔体积的含义,记住标准状况下的气体摩尔体积。3.能进行气体体积、物质的量、微粒数目之间的换算。一决定物质体积大小的因素1•在温度和压强一定时,决定物质体积大小的主要因素有:微粒的数目、微粒的大小、微粒间的距离。2.根据表格中的数据完成下列填空:状态物质密度1mol该物质的质量1mol该物质的体积结论固态Fe7.86g・cm-3(20°C)56g7.12cm3相同条件下1mol固体、液体的体积差别较大Al2.70g・cm-3(20C)27g10cm3液态H2O0.998g・cm-3(20C)18g18.04cm3H2SO41.83g・cm-3(20C)98g53.55cm3气态。21.429g・L-1(0C、101kPa)(标准状32g22.39L相同条件1mol气体的体积近似相等,在标准状况下约为22.4LH20.0899g・L-(0C、101kPa)1(标准状况)2.016g22.42L3•分析出现上述结论的原因。(1)在温度和压强一定时,任何1mol固态物质或液态物质所含微粒数目相同。微粒之间的距离很小,但微粒的大小不同,所以1mol固态物质或液态物质的体积往往是丕同的。(2)对气态物质来说:通常情况下微粒之间的距离要比微粒本身的直径大很多倍,因此,当微粒数相同时,气态物质体积的大小则主要取决于气体微粒间的距离。(3)温度和压强会较大程度地影响气体体积,当压强一定时,升高温度则微粒之间的距离变大,气体体积增大。反之,体积缩小(即通常所说的热胀冷缩);当温度一定时增大压强,微粒之间的距离减小,气体体积缩小。(4)在温度和压强一定时,微粒间的距离近似相等,因此,在相同温度和压强下,任何具有相同微粒数的气体都具有大致相同的体积。导学探夯实基础突破要点【归纳总结】1•物质体积大小的影响因素A.气体分子的大小不同B.气体分子间平均距离不同C.气体的物质的量不同D.气体的摩尔质量不同答案C二气体摩尔体积1•气体摩尔体积是单位物质的量的气体所占的体积,符号是Vm,常用的单位是L・mol-1。标准状况下,气体摩尔体积约为22.4L・mol-1。对于气体摩尔体积的理解,应注意以下几点:(1)气体摩尔体积的适用范围是气态物质。在标准状况下,1mol气体所占的体积约是22.4L。(2)气体的体积与温度、压强有关。相同温度下,单位物质的量的气体压强越小,气体体积越大:相同压强下,单位物质的量的气体温度越高,气体体积越大。(3)气体摩尔体积不仅适用于纯气体,也适用于混合气体。如0.3molH2与0.7molO2的混合气在标准状况下的体积约为22.4Lo(4)1mol气体在非标准状况下的体积,可能是22.4L,也可能不是22.4L。2.标准状况下,气体摩尔体积的有关计算2.粒子数目相同物质的体积关1•同温同压下,若两种气体所占体积不同,其主要原因是()质V①气体的物质的量n=224mol;②气体的摩尔质量M=匕JQ=22.4Qg・mol-i;V③气体的分子数N=n・NA=22TNA;V④气体的质量m=n・M=22"4'Mg。【归纳总结】1•标准状况下的气体摩尔体积条r〔在ifC*何"加瞬都阴揃22-4Lj标堆对象敎值同镒同压拒同2.计算公式V解析A中没有指明该物质所处的状况,即温度、压强,昔误;B中没有指明该物质的状态,错误;C中水在标准状况下不是气体,错误;D中是对气体摩尔体积概念的应用,正确。3•设NA代表阿伏加德罗常数,下列说法正确的是()A.在常温常压下,11.2LCl2含有的分子数为0.5NAB.在常温常压下,1mol氦气含有的原子数为NAC.32g氧气含原子数为NAD.NA个O2的质量只有在标准状况下才是32g答案B解析在A中,标准状况下,11.2LCl2含有的分子数为0.5NA,而题中为常温常压,故A错误;B中氦气为单原子分子,1mol氦气含有原子数目为N,B正确;C中O的摩尔质A2量为32g・mol-i,且O2为双原子分子,所以32gO2含原子数为一ZNA=2NA,2232g・mol-iAA错误;NA个O2的质量为32g,与状态无关,与外界条件无关,D错误。理解感悟在有关阿伏加德罗常数的正误判断题目中,常考查标准状况下的气体摩尔体积,常见问题如下:⑴忽视外界条件是标准状况,如常温常压下,1molH2的体积不是22.4L。(2)忽视研究对象是气体,如标准状况下H2O、酒精、SO3等不是气体。(3)将1mol气体的体积与气体摩尔体积的单位混淆,前者单位为L,后者单位为L・mol-U三阿伏...