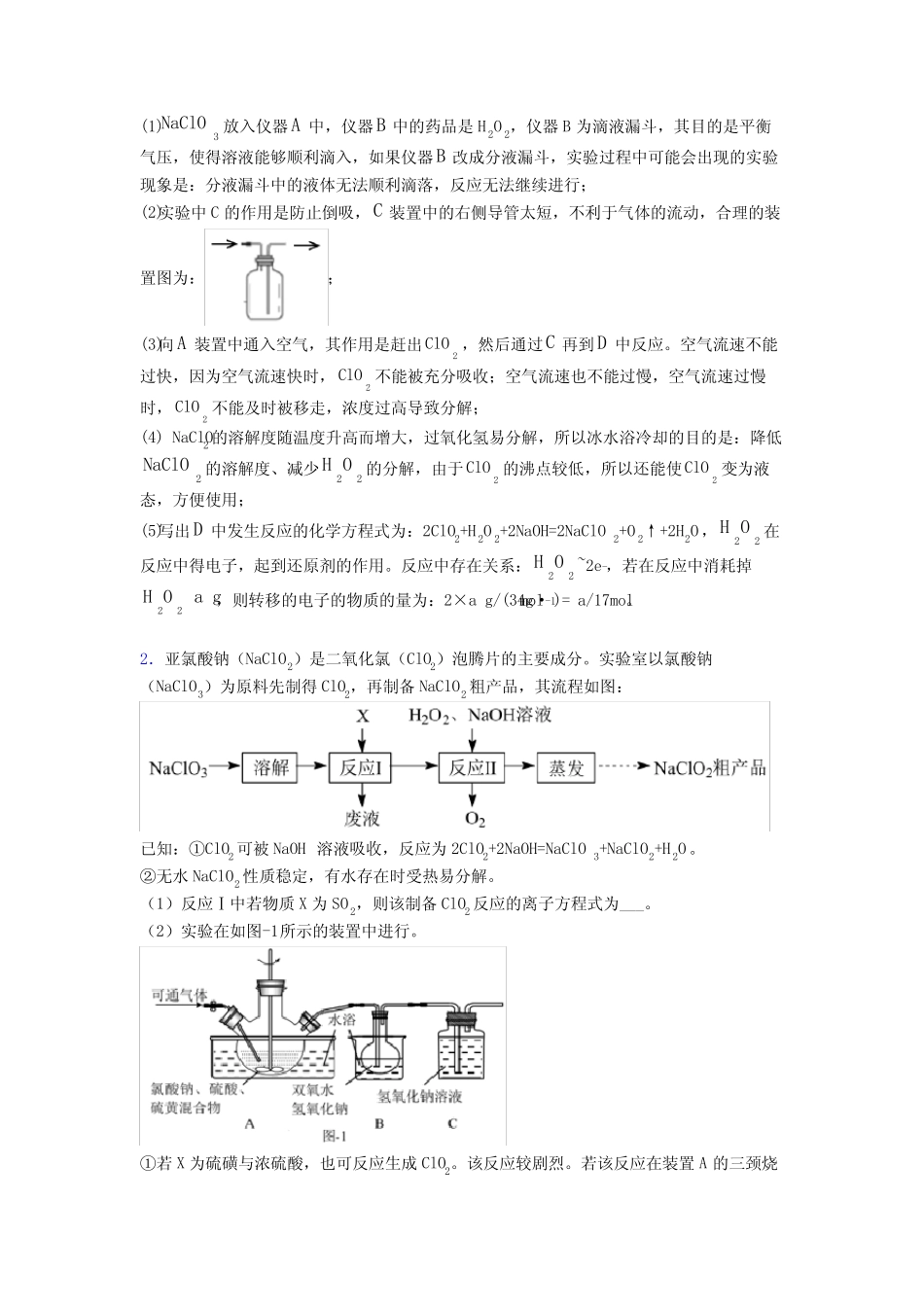
一、高中化学氧化还原反应练习题(含详细答案解析)1.2ClO是一种优良的消毒剂,浓度过高时易发生分解,为了运输和贮存便利常将其制成2NaClO固体,模拟工业上用过氧化氢法制备2NaClO固体的实验装置如图所示
已知:2ClO熔点-59℃、沸点11℃、22HO沸点150℃A中的化学方程式:32224222422NaClOHOHSO2ClOONaSO2HO(1)3NaClO放入仪器A中,仪器B中的药品是__________(写化学式)
如果仪器B改成分液漏斗,实验过程中可能会出现的实验现象__________
(2)C装置有明显缺陷,请绘出合理的装置图(标明气流方向)__________
(3)向A装置中通入空气,其作用是赶出2ClO,然后通过C再到D中反应
通空气不能过快的原因是__________,通空气也不能过慢原因是__________
(4)冰水浴冷却的目的是__________
降低2NaClO的溶解度b
减少22HO的分解c
使2ClO变为液态d
加快反应速率(5)写出D中发生反应的化学方程式__________,22HO在反应起到__________作用
假设在反应中消耗掉22HOag则有__________mol电子转移
【答案】H2O2液体无法顺利滴落空气流速快时,2ClO不能被充分吸收空气流速过慢时,2ClO不能及时被移走,浓度过高导致分解abc2ClO2+H2O2+2NaOH=2NaClO2+O2↑+2H2O还原剂a/17【解析】【分析】氯酸钠(NaClO3)在酸性条件下与过氧化氢生二氧化氯,ClO2与氢氧化钠溶液和过氧化氢发生氧化还原反应生成NaClO2,NaClO2的溶解度随温度升高而增大,通过冷却结晶,过滤洗涤得到晶体NaClO2•3H2O
【详解】(1)3NaClO放入仪器A中,仪器B中的药品是H2O2,仪器B为滴液漏斗,其目