01/12第一章化学反应的热效应章末质量评估化学反应的热效应(A)(时间:75分钟满分:100分)一、选择题:本题共16小题,共44分
第1~10小题,每小题2分;第11~16小题,每小题4分
在每小题给出的四个选项中,只有一项是符合题目要求的
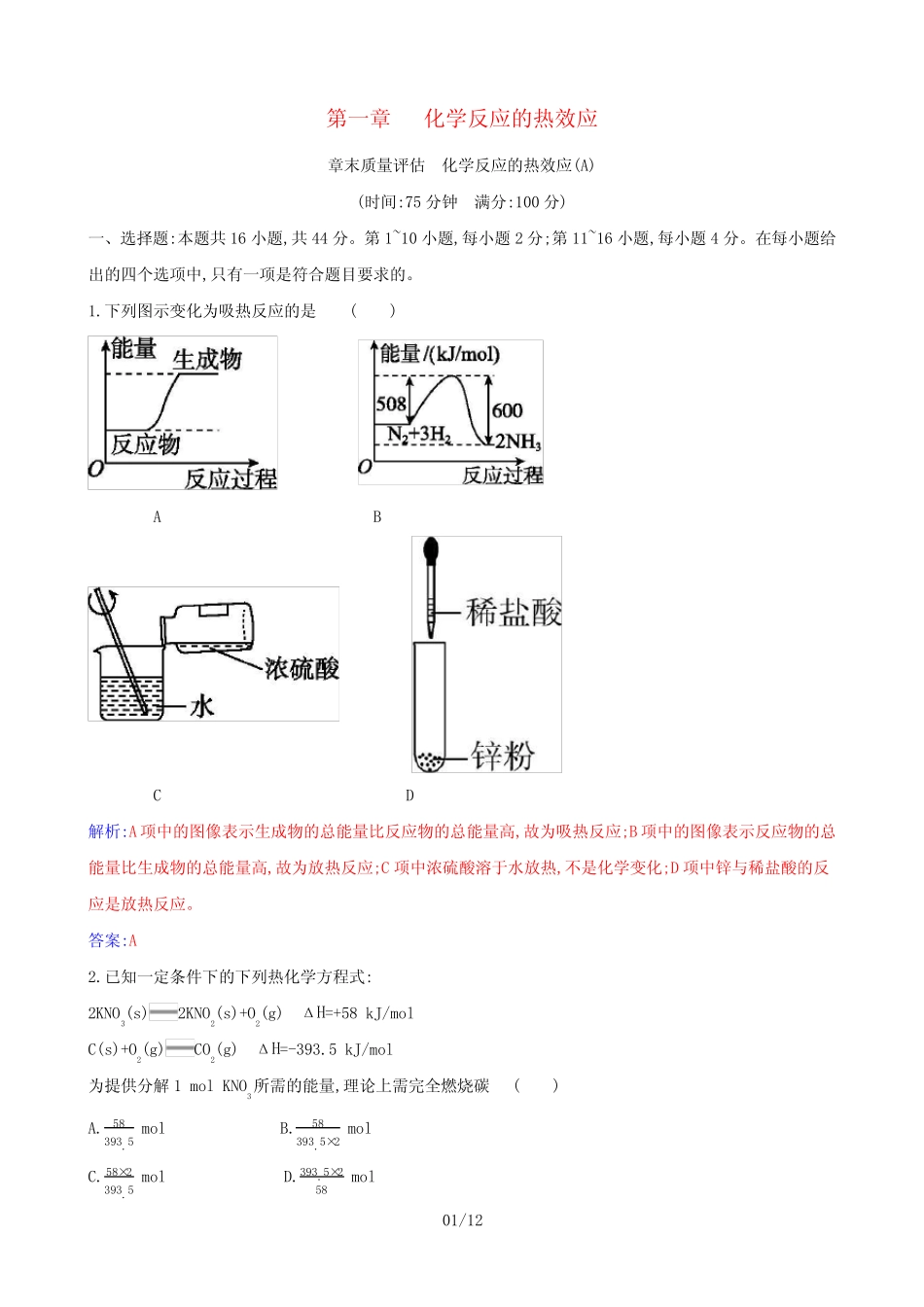
下列图示变化为吸热反应的是()ABCD解析:A项中的图像表示生成物的总能量比反应物的总能量高,故为吸热反应;B项中的图像表示反应物的总能量比生成物的总能量高,故为放热反应;C项中浓硫酸溶于水放热,不是化学变化;D项中锌与稀盐酸的反应是放热反应
已知一定条件下的下列热化学方程式:2KNO3(s)2KNO2(s)+O2(g)ΔH=+58kJ/molC(s)+O2(g)CO2(g)ΔH=-393
5kJ/mol为提供分解1molKNO3所需的能量,理论上需完全燃烧碳()A
5×2molC
58×2393
5×258mol02/12解析:依据反应2KNO3(s)2KNO2(s)+O2(g)ΔH=+58kJ/mol,分解1molKNO3所需要吸收的热量为582kJ;提供582kJ热量需要燃烧碳的物质的量为58393
5×2mol
含1molBa(OH)2的稀溶液与足量稀盐酸反应,放出热量114
表示生成1molH2O的热化学方程式是()A
Ba(OH)2(aq)+2HCl(aq)BaCl2(aq)+2H2O(l)ΔH=+114
6kJ·mol-1B
Ba(OH)2(aq)+2HCl(aq)BaCl2(aq)+2H2O(l)ΔH=-114
6kJ·mol-1C
Ba12(OH)2(aq)+HCl(aq)12BaCl2(aq)+H2O(l)ΔH=-57
3kJ·mol-1D
Ba12(OH)2(aq)+HCl(aq)12BaCl2(aq)+H2O(l)ΔH