1/16高考化学复习难点重点知识专题讲解专题八钠及其重要化合物连线高考碱金属的性质,特别是钠及其化合物(Na2O、Na2O2、NaOHNa2CO3NaHCO3)的性质是高考考查的核心内容
通常是以钠及其化合物及其它元素和化合物为载体,对化学基本概念、基本理论和考生的能力进行考查,是物质推断、鉴别及有关实验、计算的常见物质
重点、难点探源一、钠1、物理性质银白色固体,导电性能良好,密度比水小、比煤油大,熔点低,常用小刀切割
2、化学性质(1)与非金属反应4Na+O2===2Na2O,(现象:光亮的表面变暗)2Na+O2点燃Na2O2;(现象:黄色火焰,生成淡黄色固体)2Na+S===Na2S,(现象:反应剧烈,甚至爆炸)1/16(2)钠与含有酚酞的水反应现象解释2Na+2H2O===2NaOH+H2↑(3)与盐的熔融态反应TiCl4+4Na4NaCl+Ti(4)与盐溶液的反应一般不置换出金属
首先是Na与水发生反应,生成的碱再和盐发生复分解反应
如:Na投入到FeCl3溶液中:现象浮在水面上,熔成闪光的小球,产生红褐色沉淀
反应的方程式:2Na+2H2O===2NaOH+H2↑;FeCl3+3NaOH=Fe(OH)3↓+3NaCl3、钠的存在和用途钠在自然界不能以游离态存在,只能以化合态存在,主要以NaCl的形式存在
钠可用来制取Na2O2等化合物;钠、钾合金室温下呈液态,是原子反应堆的导热剂,钠是一种很强的还原剂;也可用在电光源上,如钠灯,发出黄光,射程远,透雾能力强,亮度高
4、钠的制法工业上利用电解法,以NaCl为原料来制取;因为NaCl在自然界存在广泛,易得
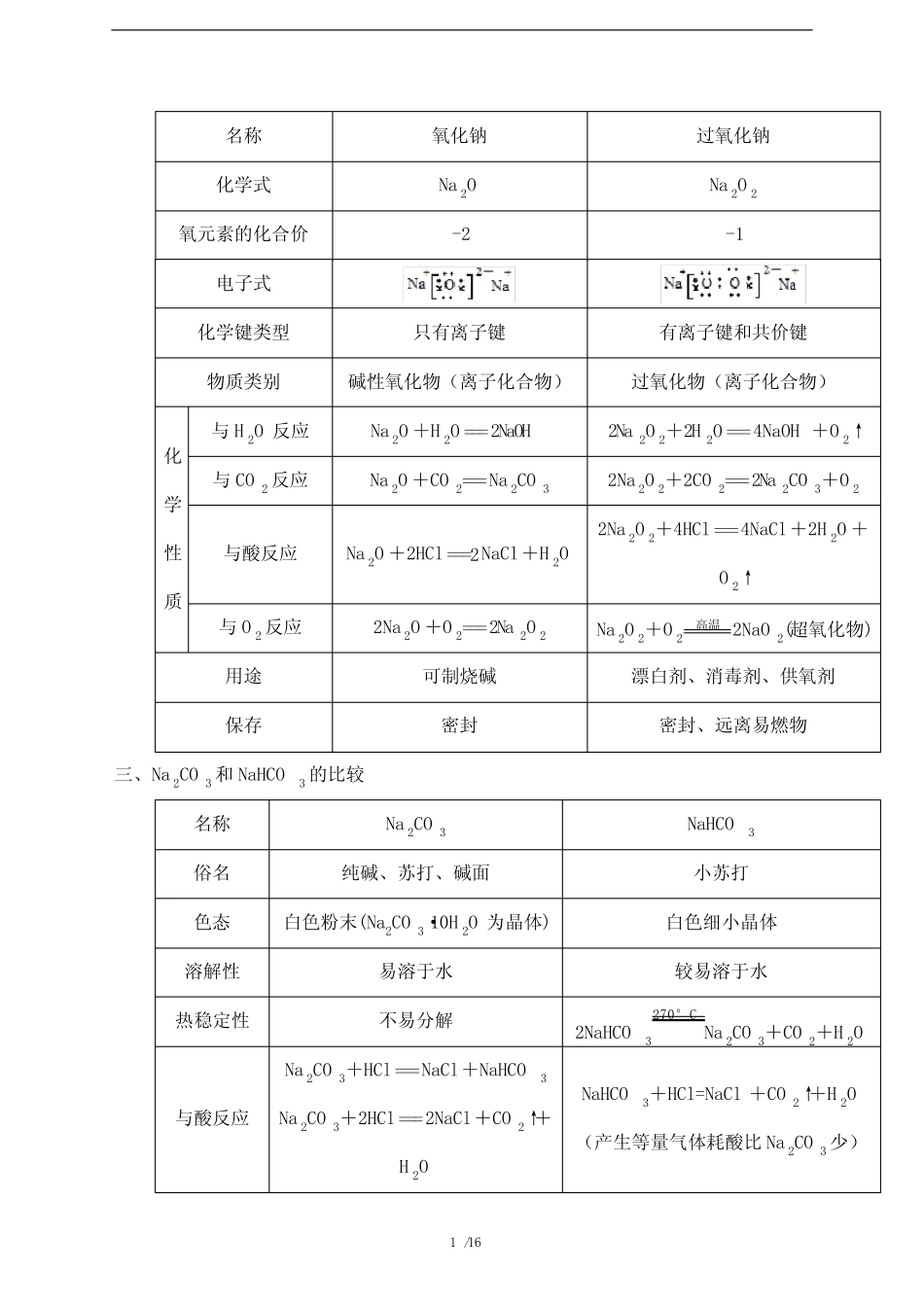
反应原理:2NaCl2Na+Cl2↑二、Na2O和Na2O2的比较电解熔融态熔融1/16名称氧化钠过氧化钠化学式Na2ONa2O2氧元素的化合价-2-1电子式化学键类型只有离子键有离子键和共价键物质类别碱性氧化物