第32讲常见气体的制备[考纲要求]1
掌握常见气体的实验室制法(包括所用试剂、仪器、反应原理和收集方法)
识别典型的实验仪器装置图
考点一气体的制备和收集1.常见气体制备的反应原理(1)O2:2KClO3=====2KCl+3O2↑或2H2O2=====2H2O+O2↑;(2)H2:Zn+H2SO4===ZnSO4+H2↑;(3)NH3:2NH4Cl+Ca(OH)2=====CaCl2+2H2O+2NH3↑;(4)CO2:CaCO3+2HCl===CaCl2+H2O+CO2↑;(5)Cl2:MnO2+4HCl(浓)=====MnCl2+Cl2↑+2H2O;(6)SO2:Na2SO3+H2SO4===Na2SO4+H2O+SO2↑;(7)NO:3Cu+8HNO3(稀)===3Cu(NO3)2+2NO↑+4H2O
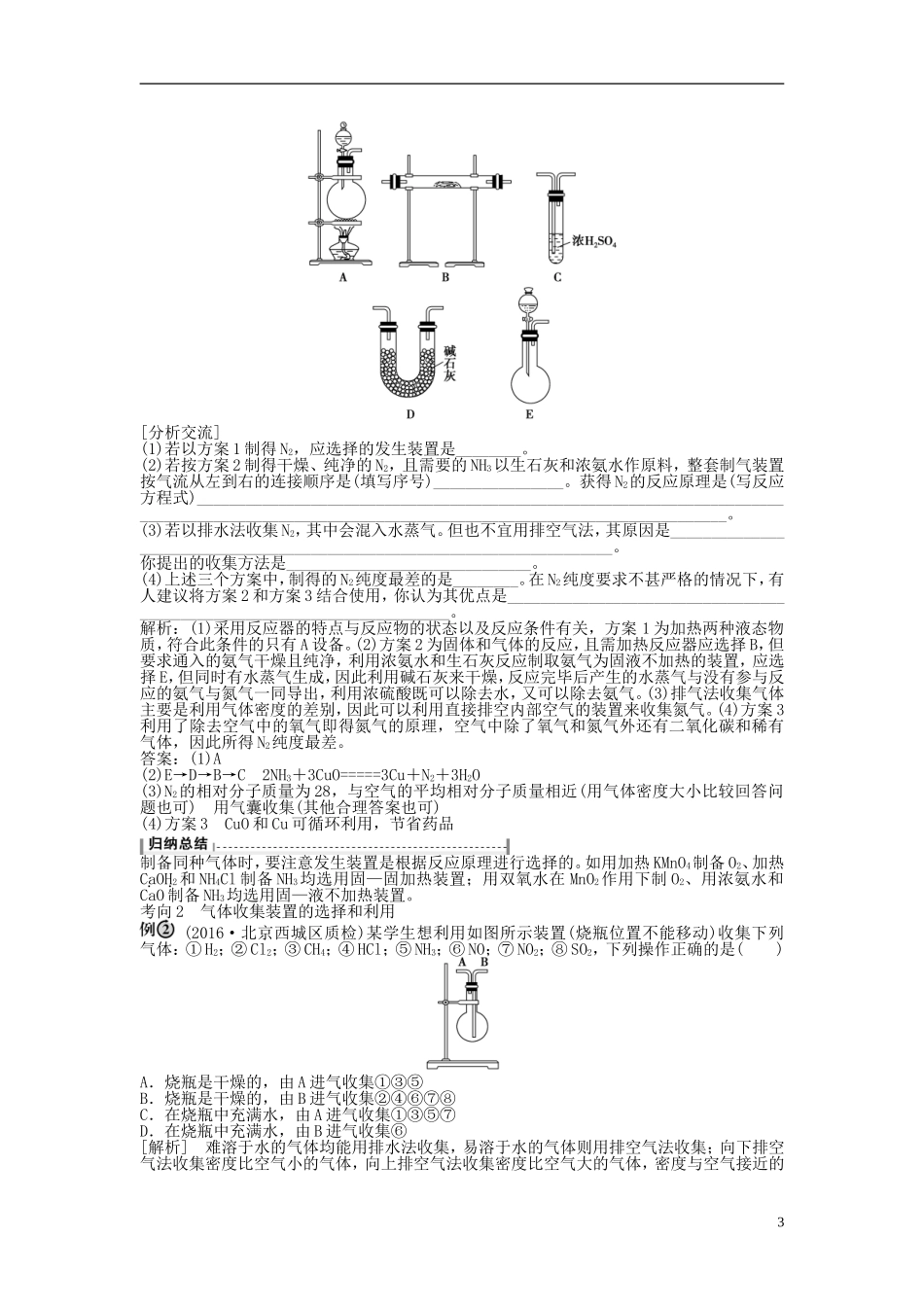
2.常见气体制备的发生装置选择反应装置一般需从反应物的状态、溶解性和反应条件确定制气装置类型,具体如表中所示:反应装置类型反应装置图适用气体操作注意事项固、固加热型O2、NH3等①试管要干燥②试管口略低于试管底③加热时先预热再固定加热④用KMnO4制取O2时,需在管口处塞一小团棉花固、液加热型或液、液加热型Cl2等①加热烧瓶时要垫石棉网②反应物均为液体时,烧瓶内要加碎瓷片加热型O2、H2、CO2、SO2、NO、NO2等①使用长颈漏斗时,要使漏斗下端插入液面以下②启普发生器只适用于块状固体和液体反应,且气体不溶于水③使用分液漏斗既可以增强气密性,又可控制液体流速和用量3
气体的收集方法收集方法排水法向上排空气法向下排空气法收集原理收集的气体不与水反应且难溶于水收集的气体密度比空气大,且与空气密度相差较大,不与空气中成分反应收集的气体密度比空气小,且与空气密度相差较大,不与空气中成分反应收集装置适用的气体H2、O2、NO、CH4Cl2、CO2、NO2、SO2H2、NH