追根知反应(1)——“氧化还原反应”相关知识全落实知识点一氧化还原反应的相关概念及表示方法1.氧化还原反应的本质和特征2.氧化还原反应的相关概念及其关系例如,反应MnO2+4HCl(浓)=====MnCl2+Cl2↑+2H2O中,氧化剂是MnO2,还原剂是HCl,氧化产物是Cl2
生成1molCl2时转移电子数目为2NA,被氧化的HCl的物质的量是2_mol,盐酸表现的性质是酸性和还原性
[提醒]元素由化合态变为游离态时,该元素不一定被还原
如:Cu2+→Cu时,铜元素被还原,Cl-→Cl2时,氯元素被氧化
3.氧化还原反应中电子转移的表示方法(1)双线桥法①表示方法写出Cu与稀硝酸反应的化学方程式并用双线桥标出电子转移的方向和数目:
②注意事项a.箭头指向反应前后有元素化合价变化的同种元素的原子,且需注明“得到”或“失去”
b.箭头的方向不代表电子转移的方向,仅表示电子转移前后的变化
c.失去电子的总数等于得到电子的总数
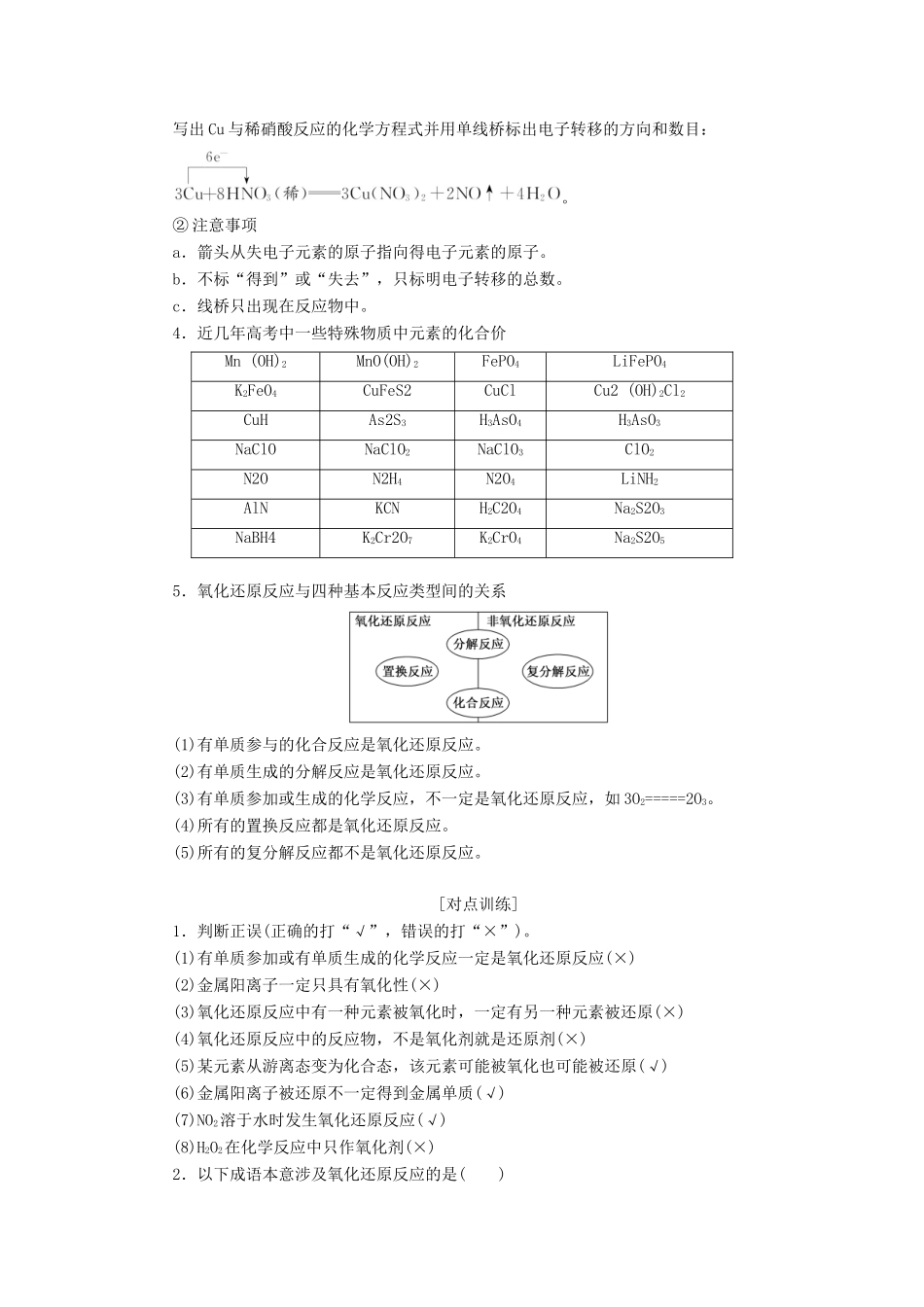
(2)单线桥法①表示方法写出Cu与稀硝酸反应的化学方程式并用单线桥标出电子转移的方向和数目:
②注意事项a.箭头从失电子元素的原子指向得电子元素的原子
b.不标“得到”或“失去”,只标明电子转移的总数
c.线桥只出现在反应物中
4.近几年高考中一些特殊物质中元素的化合价Mn(OH)2MnO(OH)2FePO4LiFePO4K2FeO4CuFeS2CuClCu2(OH)2Cl2CuHAs2S3H3AsO4H3AsO3NaClONaClO2NaClO3ClO2N2ON2H4N2O4LiNH2AlNKCNH2C2O4Na2S2O3NaBH4K2Cr2O7K2CrO4Na2S2O55.氧化还原反应与四种基本反应类型间的关系(1)有单质参与的化合反应是氧化还原反应
(2)有单质生成的分解反应是氧化还原反应
(3)有单质参加或生成的化学反应,不一定是氧化还原反应,如