元素周期律课题1-2-1元素周期律教学目标知识与技能1、掌握元素原子核外电子排布的规律2、掌握原子半径、主要化合价周期性变化3、掌握元素的金属性和非金属性随原子序数的递增而呈现周期性变化的规律过程与方法(1)自主学习,归纳比较元素周期律
(2)自主探究,通过实验探究,培养学生探究能力情感、态度与价值观学会总结,学会概括,体会结构决定性质的理念
教学重点掌握核外电子排布规律、原子半径、主要化合价、金属性和非金属性周期变化教学难点原子核外电子排布规律教学设计环节教师活动学生活动设计意图导入新课第一节我们学习了原子结构和元素性质关系,核电荷数不同的碱金属之间及卤族元素之间,在原子结构和性质上呈现一定的相似性和递变性,在其他的核电荷数不同的元素之间,是否也存在某种关系或规律呢
【板书】1.2元素周期律聆听、思考通过学过的知识引入新课
合作探究展示归纳【复习】同学们回忆原子的构成
【讲解】原子由原子核和核外电子构成,电子在核外高速绕核运动
【过渡】有的同学就要想了,多个电子运动会不会出现碰撞,那电子运动的轨迹是怎么样的呢
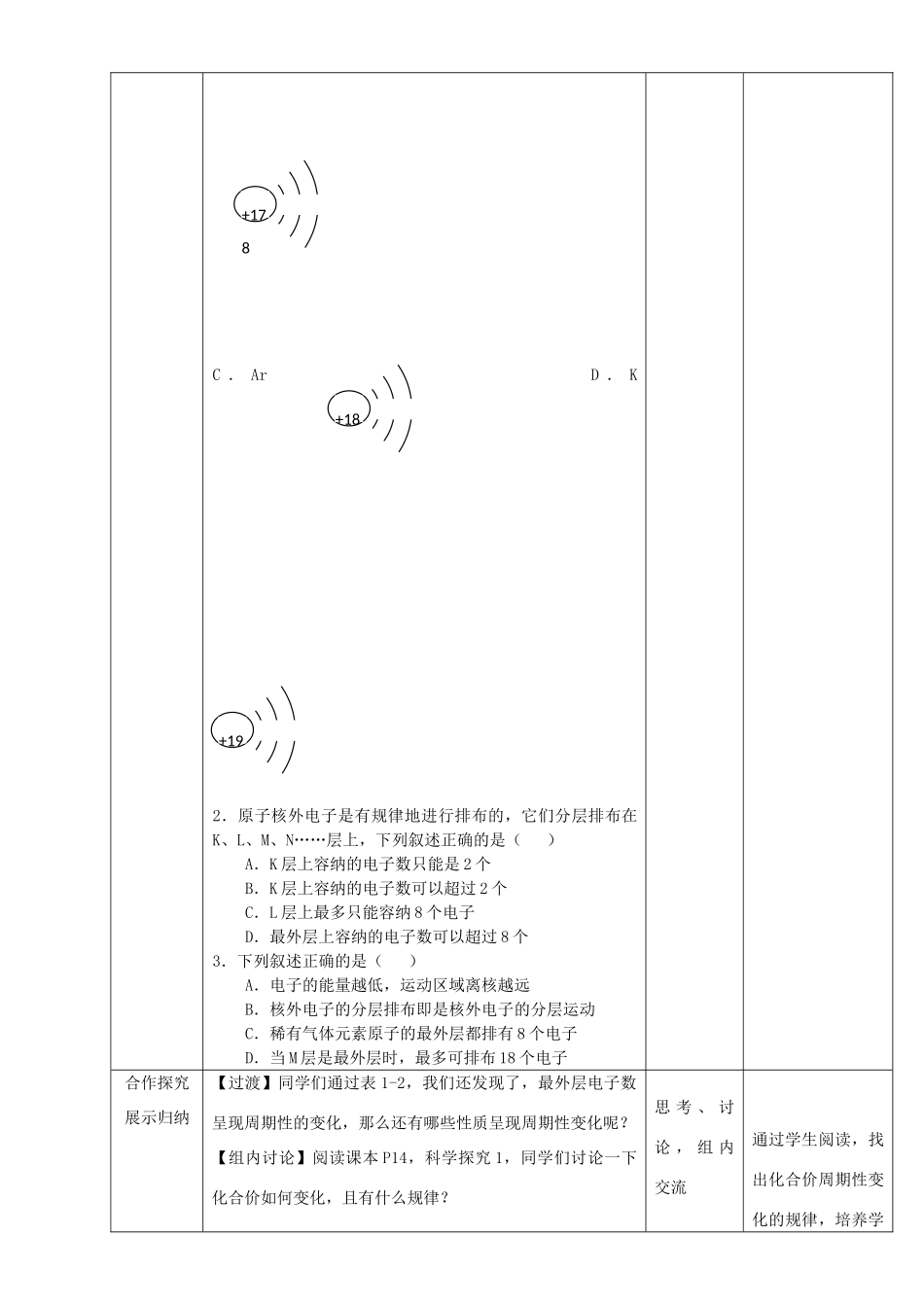
【板书】一、原子核外电子的排布【阅读】阅读课本P13页表1-2,小结出原子核外电子排布规律思考以下问题:(1)根电子层最多容纳_________个电子;(2)最外层电子数不超过______个电子(K层为最外层时不超过______个);(3)次外层电子数不超过_______个电子;学生回忆知识,并回答
学生阅读课本,完成问题
通过学过的知识,引入核外电子排布规律
通过学生阅读课本,完成问题,培养学生总结归纳能力
(4)核外电子总是尽先排布在能量_____的电子层,然后由里向外,依次排布在能量逐步_____的电子层
【板书】1.电子层(n)1234567符号KLMNOPQ离核远近近→远能量高低低→高2.一般规律(1)核外电子总是尽可能排布在能量低的电子层里,然后排布在能