第七章硅和硅酸盐工业第一节碳族元素[基础知识]一
包括元素:碳(6C),硅(14Si),锗(32Ge),锡(50Sn),铅(82Pb)2
在周期表中的位置:第ⅣA族,第2-6周期
原子结构特点:最外层有4个电子
元素性质的变化规律
元素符号核电荷数原子半径主要化合价单质的性质颜色状态密度熔点C6增大+2,+4金刚石:无色石墨:灰黑色C60固体增大减小Si14+2,+4晶体硅:灰黑色固体Ge32+2,+4银灰色固体937
4℃Sn50+2,+4银白色固体231
9℃Pb82+2,+4蓝白色固体327
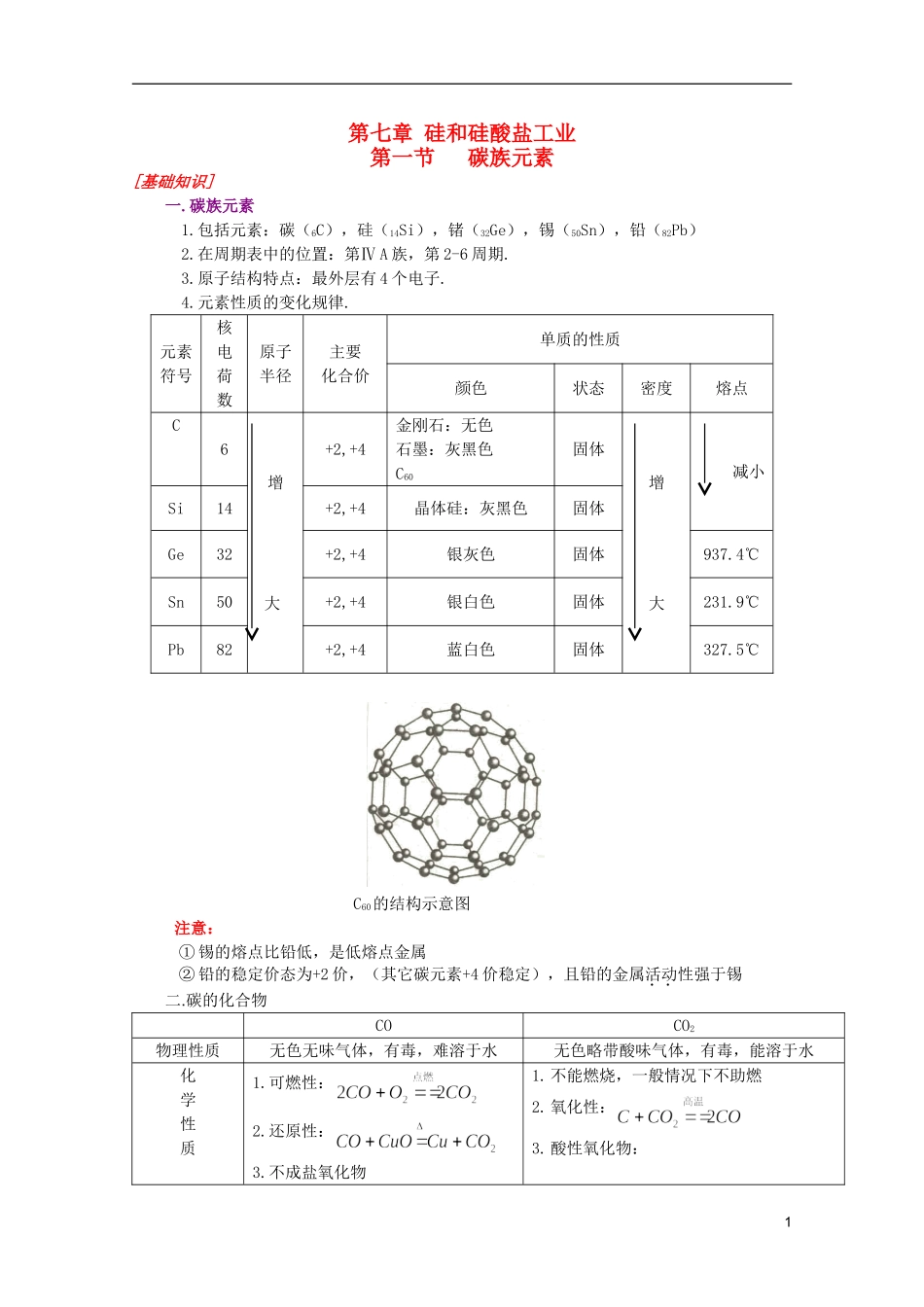
5℃C60的结构示意图注意:①锡的熔点比铅低,是低熔点金属②铅的稳定价态为+2价,(其它碳元素+4价稳定),且铅的金属活动性强于锡二
碳的化合物COCO2物理性质无色无味气体,有毒,难溶于水无色略带酸味气体,有毒,能溶于水化学性质1
不成盐氧化物1
不能燃烧,一般情况下不助燃2
酸性氧化物:1实验室制法略检验方法点燃后在火焰上方罩上干燥的烧杯和沾有澄清石灰水的烧杯,出现浑浊使澄清的石灰水变浑浊三
在自然界中的存在形态:化合态(没有游离态)2
同素异形体:晶体硅,无定形硅3
物理性质:晶体硅是灰黑色,有金属光泽,熔点高,硬而脆的固体,具有单向导电性,是良好的半导体材料4
化学性质:晶体硅在常温下化学性质不活泼,无定形硅比晶体硅活泼,其主要化学性质如下:①与非金属反应:1)Si在常温下只能与F2反应Si+2F2=SiF4(气体)2)Si在高温下能与其它卤素和非金属单质反应:400℃时(液态)600℃时(研细的Si在氧气中燃烧,放出大量的热)1300℃时与N2反应得Si3N4(氮化硅),氮化硅陶瓷是一种重要的结构材料,在2000℃时与碳反应生成SiC,它是无色晶体,具有金刚石结构,又名金刚砂
②与酸反应:常温时硅不与H