化学实验方案的设计复习临沂高新实验中学尹克平教学目标知识技能:以铁的化合物的制备和性质为主线,加深对Fe、Fe2+、Fe3+之间的氧化还原反应以及复分解反应知识的理解
能力培养:训练根据实验目的及原理,选择合适的仪器和药品,设计可行的操作步骤,确定实验的观察重点,写出完整的实验报告的实验技能
科学情感:培养根据实验的要求,设计制备实验和性质实验两种实验方案的实验能力
科学方法:培养认真严谨的科学态度,科学、合理、周密、安全的实施化学实验
重点、难点:制备实验方案的设计以及性质实验方案的设计
教学过程设计教师活动【介绍】化学实验方案的设计在化学科学的发现中起到过很重要的作用
如镭和碳-60的发现等
实验方案的设计是在实施化学实验之前,对实验进行的一种规划,主要内容是什么
学生活动【回答】根据化学实验的目的和要求,运用相关化学知识和技能,对实验的仪器、装置和方法进行的一种规划
【引入】这节课,我们要进行实验方案的设计是:1.以还原铁粉为原料制备Fe(OH)2并观察它在空气中的氧化过程
2.红砖中氧化铁成分的检验
【启发】我们先对第1个课题的实验原理、实验步骤、实验方法依次地进行讨论
1.分析实验的化学原理【讨论】2.确定实验的具体步骤【讨论】①将还原铁粉氧化Fe2+的溶液;②用Fe+的溶液与碱溶液反应生成Fe(OH)2沉淀;③使Fe(OH)2在空气中氧化成Fe(OH)3
将Fe→Fe2+,可以采取几个方案
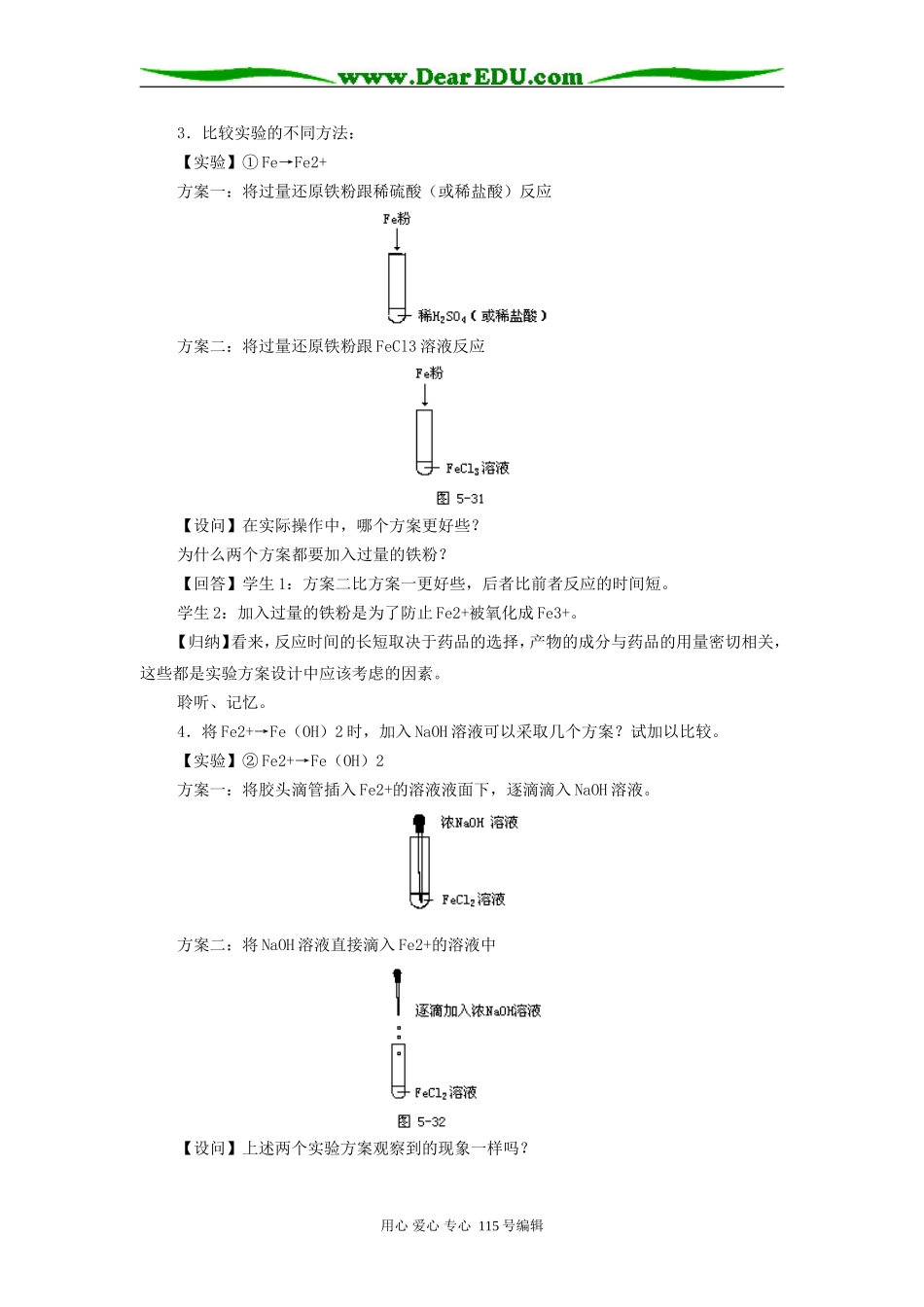
用心爱心专心115号编辑3.比较实验的不同方法:【实验】①Fe→Fe2+方案一:将过量还原铁粉跟稀硫酸(或稀盐酸)反应方案二:将过量还原铁粉跟FeCl3溶液反应【设问】在实际操作中,哪个方案更好些
为什么两个方案都要加入过量的铁粉
【回答】学生1:方案二比方案一更好些,后者比前者反应的时间短
学生2:加入过量的铁粉是为了防止Fe2+被氧化成Fe3+