高考化学高频物质——焦亚硫酸钠(Na2S2O5)1
外观与性状:为无色棱柱状结晶或白色粉末;有二氧化硫味、酸、咸、;贮存日久色渐变黄
熔点(℃):>300(分解)相对密度(水=1):1
溶解性:溶于水,水溶液呈酸性(20℃时为54g/100ml水;100℃时为81
7g/100ml水)
溶于甘油,微溶于乙醇
溶于水溶于甘油,微溶于乙醇
受潮易分解,露置空气中易氧化成硫酸钠
与强酸接触放出二氧化硫而生成相应的盐类
加热到150℃分解
稳定性和反应活性禁配物:强酸、强氧化剂
避免接触的条件:潮湿空气5
物化性质:焦亚硫酸钠为白色或黄色结晶粉末或小结晶,带有强烈的SO2气味,比重1
4,溶于水,水溶液呈酸性,与强酸接触则放出SO2而生成相应的盐类,久置空气中,则氧化成Na2S2O6,故该产品不能久存
高于150℃,即分解出SO2
1.【2014·福建理综化学卷,T25】(15分)焦亚硫酸钠(Na2S2O5)是常用的食品抗氧化剂之一
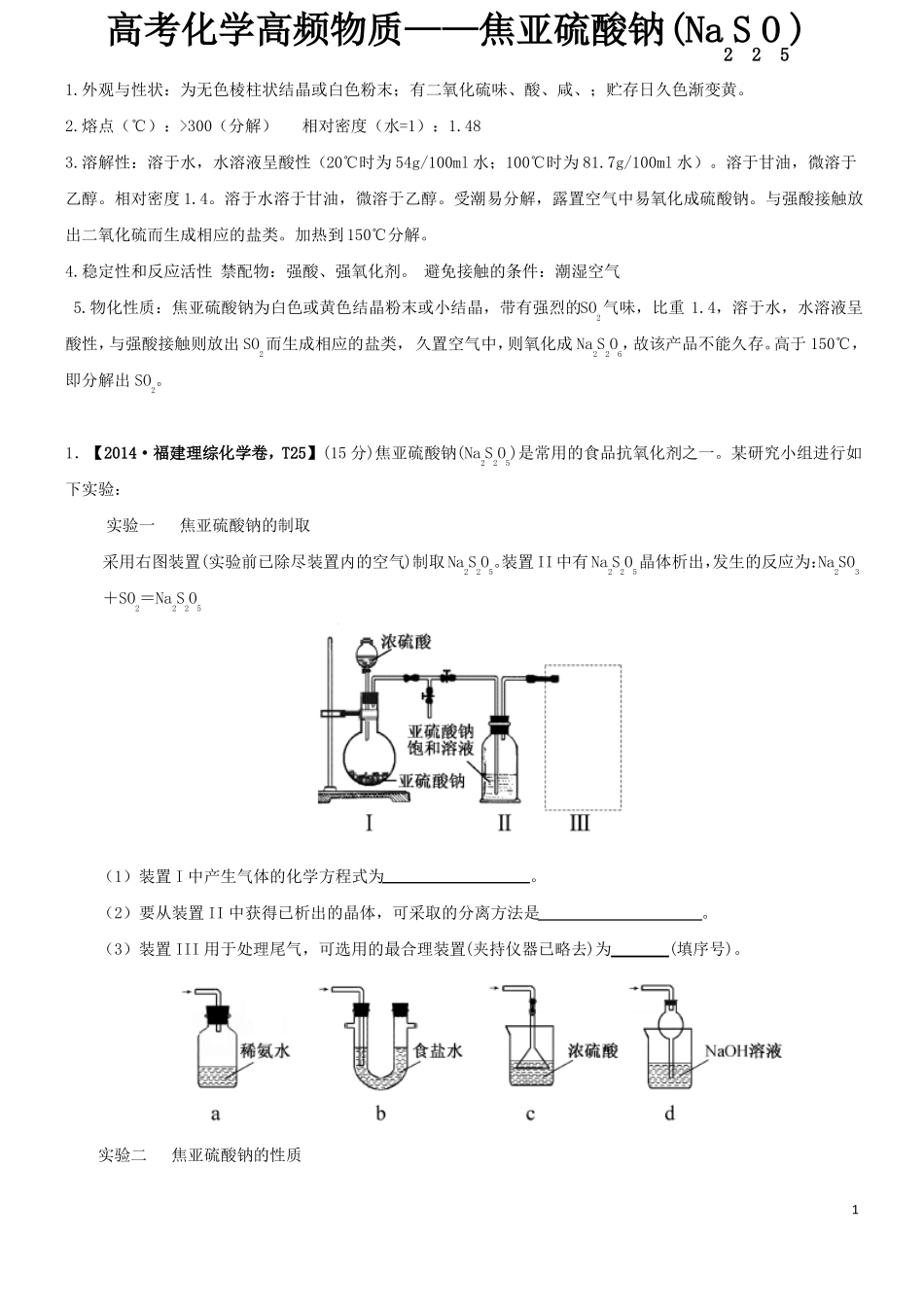
某研究小组进行如下实验:实验一焦亚硫酸钠的制取采用右图装置(实验前已除尽装置内的空气)制取Na2S2O5
装置II中有Na2S2O5晶体析出,发生的反应为:Na2SO3+SO2=Na2S2O5(1)装置I中产生气体的化学方程式为
(2)要从装置II中获得已析出的晶体,可采取的分离方法是
(3)装置III用于处理尾气,可选用的最合理装置(夹持仪器已略去)为(填序号)
实验二焦亚硫酸钠的性质1Na2S2O5溶于水即生成NaHSO3
(4)证明NaHSO3溶液中HSO3的电离程度大于水解程度,可采用的实验方法是(填序号)
a.测定溶液的pHb.加入Ba(OH)2溶液c.加入盐酸d.加入品红溶液e.用蓝色石蕊试纸检测(5)检验Na2S2O5晶体在空气中已被氧化的实验方案是
实验三葡萄酒中抗氧化剂残留量的测定(6)葡萄酒常用Na2