化学反应与能量变化2叮叮叮叮叮口3叮叮叮叮叮4叮叮叮叮5叮叮叮叮6叮叮叮叮叮叮叮自检自查必考点反应热的本质、类型及图像识别:ODDDDDDDDDDDDDDDDDDDDDDDDDDDDDDDDDDDDDDDDDDDDDDDDDDDDDDDDDDDDDDDDDDDDDDDDDDDDDDDDDDDDDDDDDDDDD①DDDDDDDDDDDDDDDDDDDDDDDDDD②DDDDDDDDDDDD放热反应:DDDDDDDDDDDDDDDD△H生成物的总能量反应物的总键能0反应物的总能量生成物的总键能DDD①DDDDDDDDCaCO3^~CaO+CO2T②2NH4Cl(s)+Ba(OH)2^8H2O(s)===BaCl2+2NH3T+10H2O□C(s)+H2O(g)YO+H2DCOc+CTCODDDDDDDDDDDDDDDNH+DDD4A
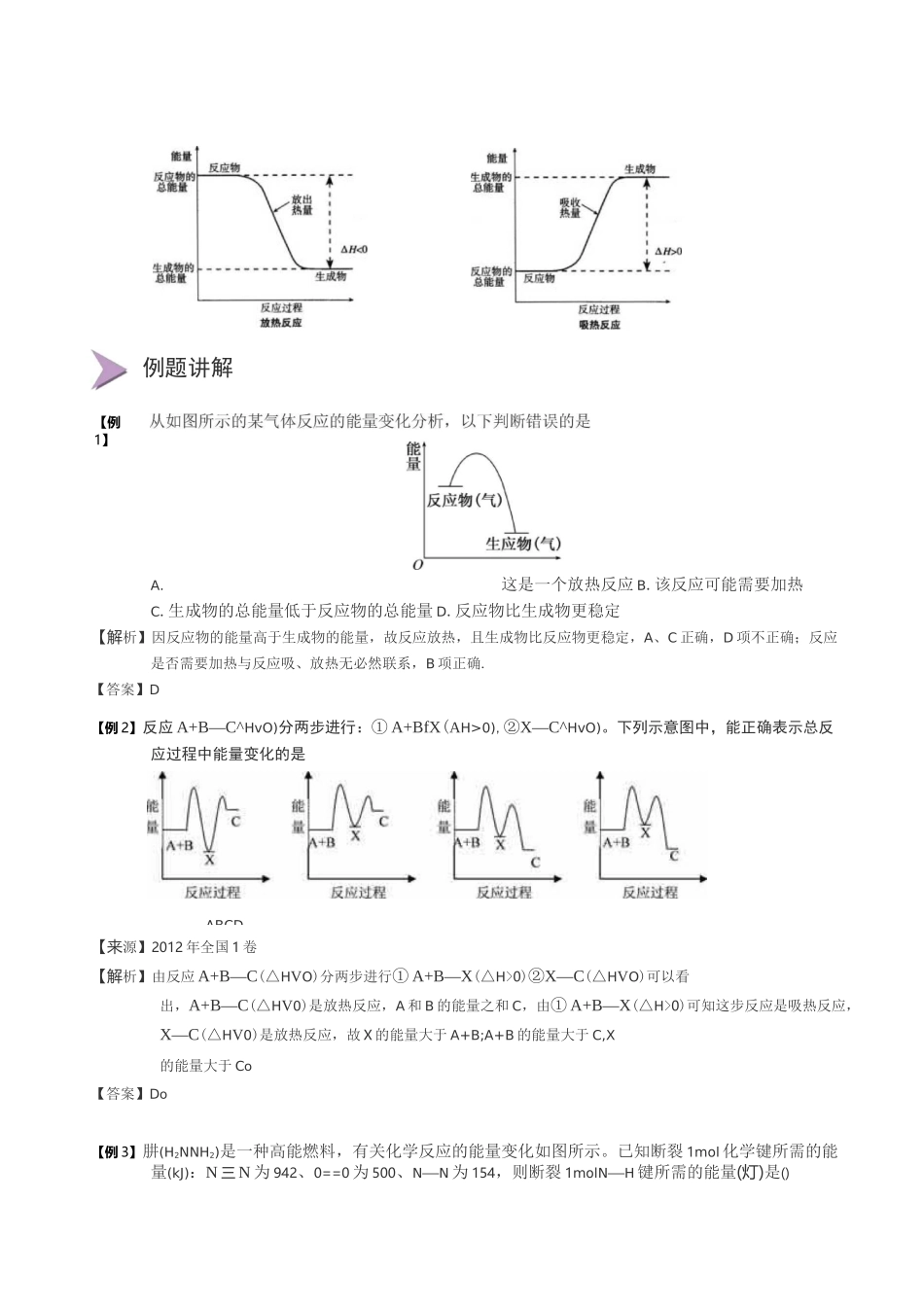
这是一个放热反应B
该反应可能需要加热C
生成物的总能量低于反应物的总能量D
反应物比生成物更稳定【解析】因反应物的能量高于生成物的能量,故反应放热,且生成物比反应物更稳定,A、C正确,D项不正确;反应是否需要加热与反应吸、放热无必然联系,B项正确
【答案】D【例2】反应A+B—C^HvO)分两步进行:①A+BfX(AH>0),②X—C^HvO)
下列示意图中,能正确表示总反应过程中能量变化的是【来源】2012年全国1卷【解析】由反应A+B—C(△HVO)分两步进行①A+B—X(△H>0)②X—C(△HVO)可以看出,A+B—C(△HV0)是放热反应,A和B的能量之和C,由①A+B—X(△H>0)可知这步反应是吸热反应,X—C(△HV0)是放热反应,故X的能量大于A+B;A+B的能量大于C,X的能量大于Co【答案】Do【例3】肼(H2NNH2)是一种高能燃料,有关化学反应的能量变化如图所示
已知断裂1mol化学键所需的能量(kJ):N三N为942