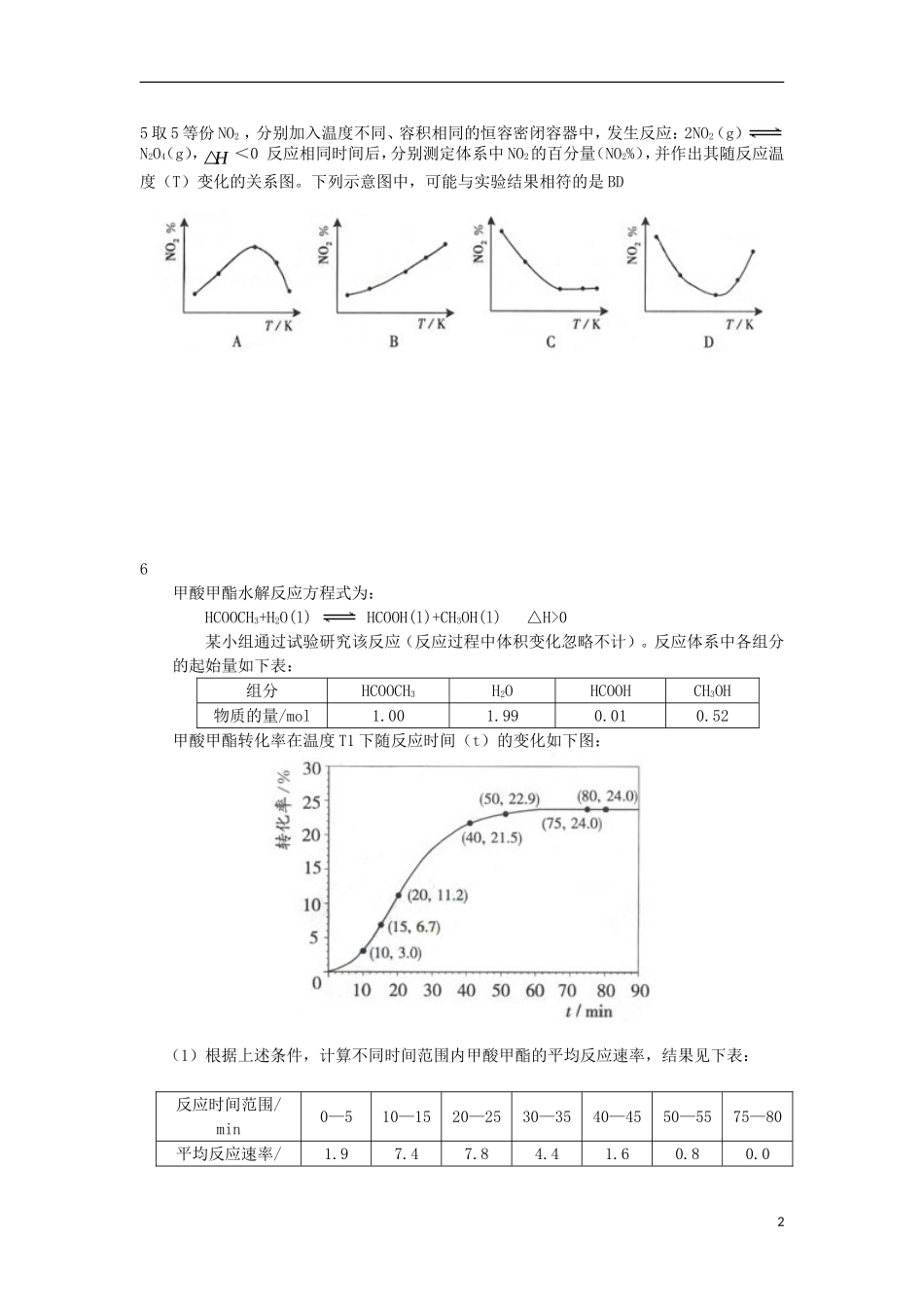
化学能力训练(10)1某探究小组利用丙酮的溴代反应(CH3COCH3+Br2→CH3COCH2Br+HBr)来研究反应物浓度与反应速率的关系
反应速率通过测定溴的颜色消失所需的时间来确定
在一定温度下,获得如下实验数据:实验序号初始浓度c/mol·L—1溴颜色消失所需时间t/s①②③④CH3COCH3HC1Br30
0020290145145580分析实验数据所得出的结论不正确的是A.增大增大B.实验②和③的相等C.增大增大D.增大,增大2在25℃时,密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如下表:物质XYZ初始浓度/mol·L-10
20平衡浓度/mol·L-10
1下列说法错误的是A.反应达到平衡时,X的转化率为50%B.反应可表示为X+3Y2Z,其平衡常数为1600C.增大压强使平衡向生成Z的方向移动,平衡常数增大D.改变温度可以改变此反应的平衡常数3已知汽车尾气无害化处理反应为2NO(g)+2CO(g)N2(g)+2CO2(g)下列说法不正确的是A.升高温度可使该反应的逆反应速率降低B.使用高效催化剂可有效提高正反应速率C.反应达到平衡后,N0的反应速率保持恒定D.单位时间内消耗CO和CO2的物质的量相等时,反应达到平衡4难挥发性二硫化钽(TaS2)可采用如下装置提纯
将不纯的TaS2粉末装入石英管一端,抽真空后引入适量碘并封管,置于加热炉中
反应如下:TaS2(s)+2l2(g)Tal4(g)+S2(g)下列说法正确的是A.在不同温度区域,Tal4的量保持不变B.在提纯过程中,l2的量不断减少C.在提纯过程中,l1的作用是将TaS2从高温区转移到低温区D.该反应的平衡常数与Tal4和S2的浓度乘积成反比11123k1023k5取5等份N