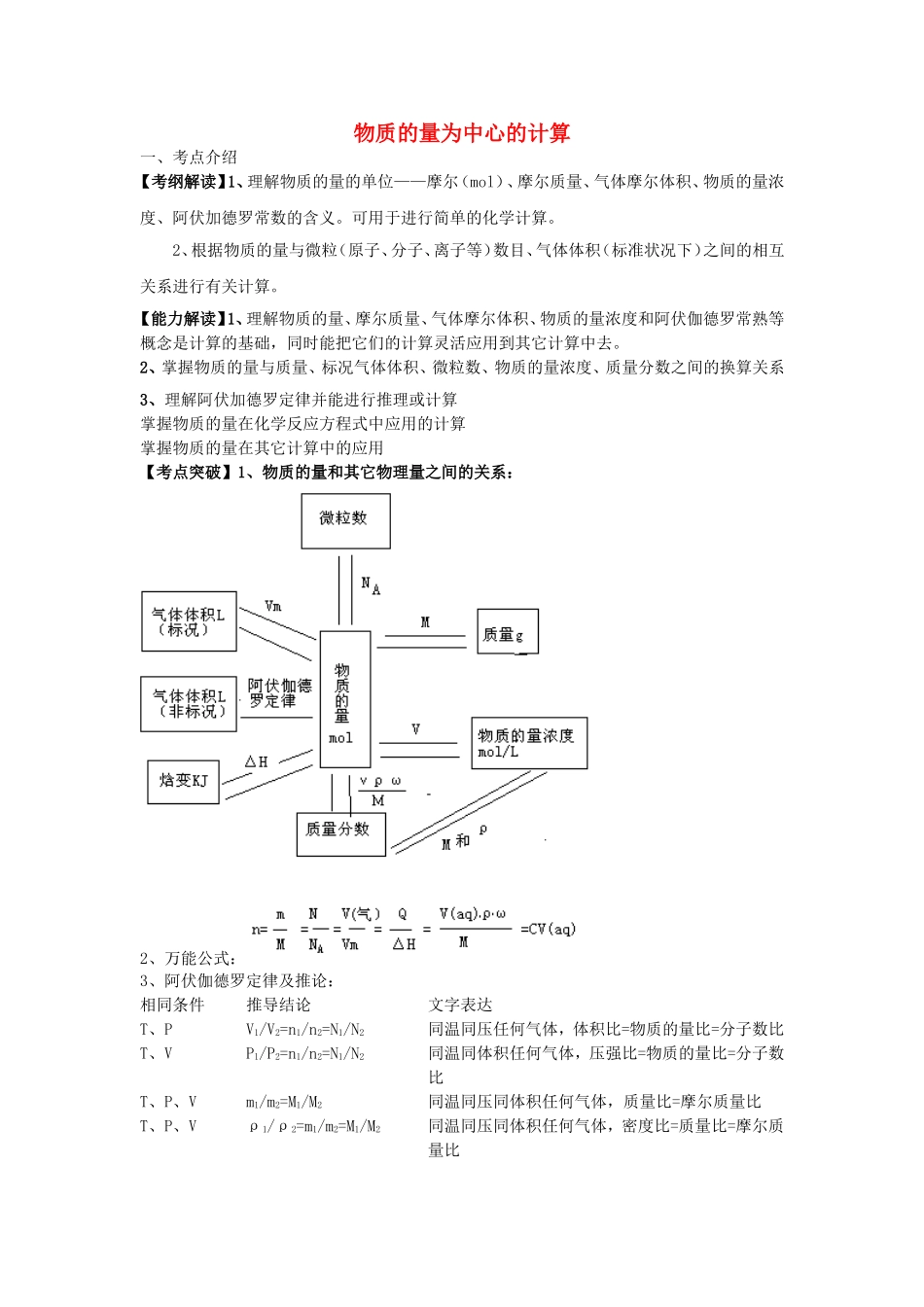
物质的量为中心的计算一、考点介绍【考纲解读】1、理解物质的量的单位——摩尔(mol)、摩尔质量、气体摩尔体积、物质的量浓度、阿伏加德罗常数的含义。可用于进行简单的化学计算。2、根据物质的量与微粒(原子、分子、离子等)数目、气体体积(标准状况下)之间的相互关系进行有关计算。【能力解读】1、理解物质的量、摩尔质量、气体摩尔体积、物质的量浓度和阿伏伽德罗常熟等概念是计算的基础,同时能把它们的计算灵活应用到其它计算中去。2、掌握物质的量与质量、标况气体体积、微粒数、物质的量浓度、质量分数之间的换算关系3、理解阿伏加德罗定律并能进行推理或计算掌握物质的量在化学反应方程式中应用的计算掌握物质的量在其它计算中的应用【考点突破】1、物质的量和其它物理量之间的关系:2、万能公式:3、阿伏伽德罗定律及推论:相同条件推导结论文字表达T、PV1/V2=n1/n2=N1/N2同温同压任何气体,体积比=物质的量比=分子数比T、VP1/P2=n1/n2=N1/N2同温同体积任何气体,压强比=物质的量比=分子数比T、P、Vm1/m2=M1/M2同温同压同体积任何气体,质量比=摩尔质量比T、P、Vρ1/ρ2=m1/m2=M1/M2同温同压同体积任何气体,密度比=质量比=摩尔质量比T、P、mρ1/ρ2=V2/V1=n2/n1同温同压同质量任何气体,密度和体积成反比;密度和物质的量成反比【考查方向】;1选择题:常考查物质的量、阿伏伽德罗常熟、物质的量浓度、阿伏伽德罗定律、气体摩尔体积的概念的理解;物质的量的计算在其它计算中的应用的简单计算;围绕物质的量为中心的简单计算的机械组合型选择题和利用物质的量在其它计算中的应用是两种常见类型。2:主观题:很少有单独考查计算的试题,主要是利用物质的量作为工具进行简单计算或综合计算部分工具。二、高考真题1.浓度为0.50mol·L-1的某金属阳离子Mn+的溶液10.00mL,与0.40mol·L-1的NaOH溶液12.50mL完全反应,生成沉淀,则n等于A1B2C3D4〖解析〗:n×10.00mL×0.50mol·L-1=12.50Ml×0.40mol·L-1,n=1〖答案〗:A2.同温同压下,在3支相同体积的试管中分别充有等体积混合的2种气体,它们是①NO和NO2,②NO2和O2,③NH3和N2。现将3支试管均倒置于水槽中,充分反应后,试管中剩余气体的体积分别为V1、V2、V3,则下列关系正确的是AV1>V2>V3BV1>V3>V2CV2>V3>V1DV3>V1>V2〖解析〗:3NO2+H2O=2HNO3+NO,4NO2+O2+2H2O=4HNO3,设试管的体积为2,根据方程式。V1=4/3;V2=3/4;V3=1,〖答案〗:B3.是一种广谱型的消毒剂,根据世界环保联盟的要求ClO2将逐渐取代Cl2成为生产自来水的消毒剂。工业上ClO2常用NaClO3和Na2SO3溶液混合并加H2SO4酸化后反应制得,在以上反应中NaClO3和Na2SO3的物质的量之比为A1︰1B2︰1C1︰2D2︰3〖解析〗:根据电子得失守恒n(NaClO3)=2n(Na2SO3)〖答案〗:B4、在一定条件下,1体积气体A2和3体积气体B2完全反应生成了2体积气体X(体积在相同条件下测定),则X的化学式是AABBA2B3CAB2DAB3〖解析〗:根据阿伏伽德罗定律,A2+3B2=2X,所以平均每个分子含有1个A原子,三个B原子。〖答案〗:D5、在273K和101kPa的条件下,将2.00g氦气、1.40g氮气和1.60g氧气混合,该混合气体的体积是A.6.72LB.7.84LC.10.08LD.13.44L〖解析〗:2.00g氦气、1.40g氮气和1.60g氧气的物质的量分别是0.5mol、0.05mol、0.05mol,总物质的量为0.6mol,则在273K和101kPa的条件下为0.6mol×22.4L/mol=13.44L〖答案〗:D6.设NA代表阿伏加德罗常数,下列说法正确的是A.5.6g铁与足量盐酸反应转移的电子数为0.3NAB.100mL2.0mol/L的盐酸与醋酸溶液中氢离子均为0.2NAC.标准状况下,22.4L氦气与22.4L氟气所含原子数均为2NAD.20g重水(D2O)中含有的电子数为10NA〖解析〗:A错,因为Fe和盐酸反应氧化产物是Fe2+,5.6g铁失去电子数为0.2NAB错,因为醋酸是弱酸不完全电离,氢离子小于0.2NAC错,氦气是单原子分子,所含原子数均为NA〖答案〗:D7等量镁铝合金粉末分别与下列4种过量的溶液充分反应,放出氢气最多的是A.2mol·L-1H2SO4溶液B.18mol·L-1H2SO4溶液C.6mol·L-1KOH溶液D.3mol·L-1HNO3溶液〖解析〗:B钝化;D不产生氢气;C不与Mg反应,A与镁铝都反应产生氢气。〖答案〗:A8.用...