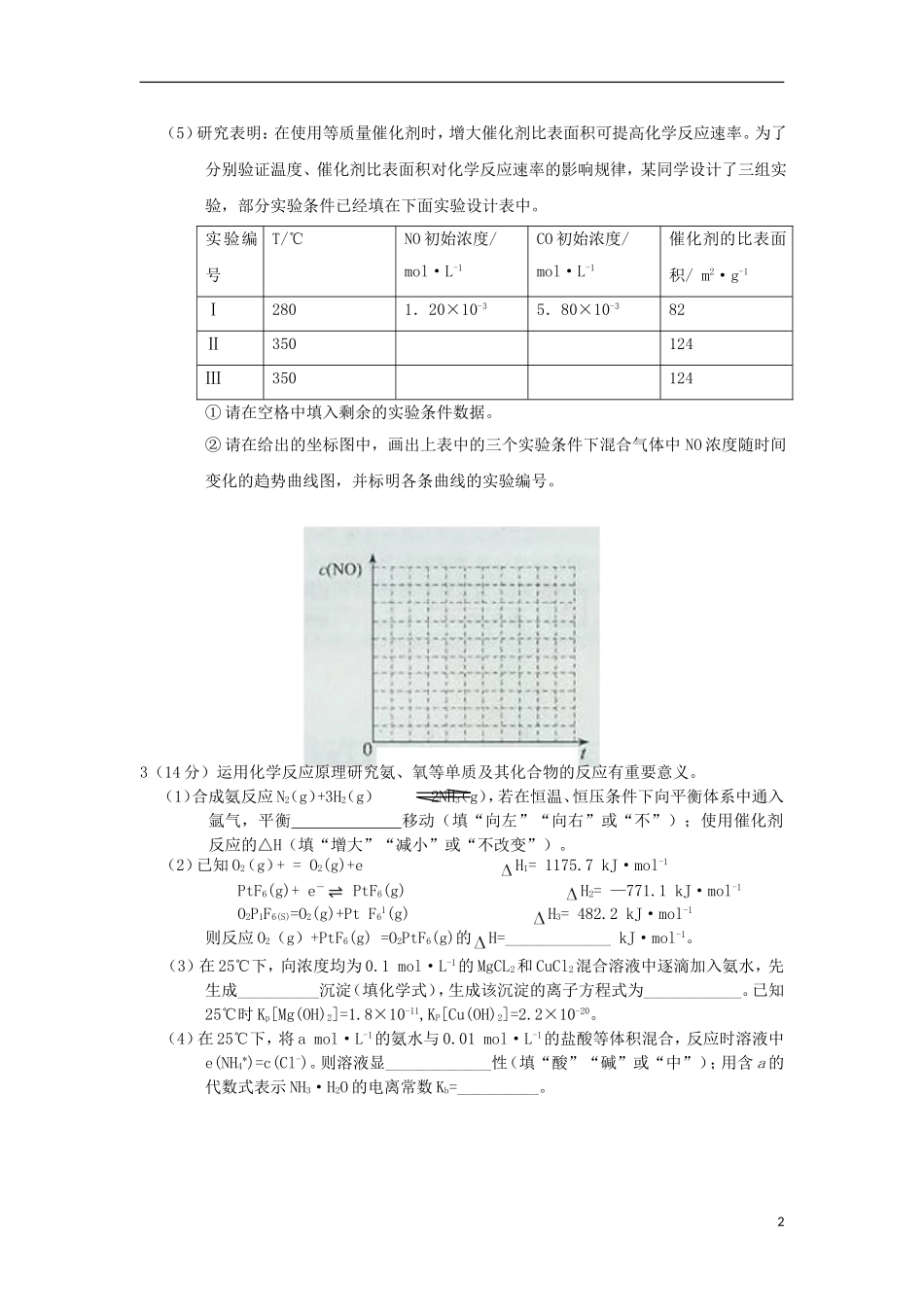
化学能力训练(11)1(14分)运用化学反应原理研究氨、氧等单质及其化合物的反应有重要意义
(1)合成氨反应N2(g)+3H2(g)2NH3(g),若在恒温、恒压条件下向平衡体系中通入氩气,平衡移动(填“向左”“向右”或“不”);使用催化剂反应的△H(填“增大”“减小”或“不改变”)
(2)已知O2(g)+=O2(g)+eH1=1175
7kJ·mol-1PtF6(g)+e-PtF6(g)H2=—771
1kJ·mol-1O2P1F6(S)=O2(g)+PtF61(g)H3=482
2kJ·mol-1则反应O2(g)+PtF6(g)=O2PtF6(g)的H=_____________kJ·mol-1
(3)在25℃下,向浓度均为0
1mol·L-1的MgCL2和CuCl2混合溶液中逐滴加入氨水,先生成__________沉淀(填化学式),生成该沉淀的离子方程式为____________
已知25℃时Kp[Mg(OH)2]=1
8×10-11,KP[Cu(OH)2]=2
2×10-20
(4)在25℃下,将amol·L-1的氨水与0
01mol·L-1的盐酸等体积混合,反应时溶液中e(NH4*)=c(Cl-)
则溶液显_____________性(填“酸”“碱”或“中”);用含a的代数式表示NH3·H2O的电离常数Kb=__________
2(15分)超音速飞机在平流层飞行时,尾气中的NO会破坏臭氧层
科学家正在研究利用催化技术将尾气中的NO和CO转变成CO2和2CO2的化学方程式如下:2NO+2CO2CO2+N2为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如表:时间/s012345c(CO)/mol·L-11.00×10-34.50×10-42.50×10-41.50×10-41.00×10-41.00×10-4c(CO)/mo