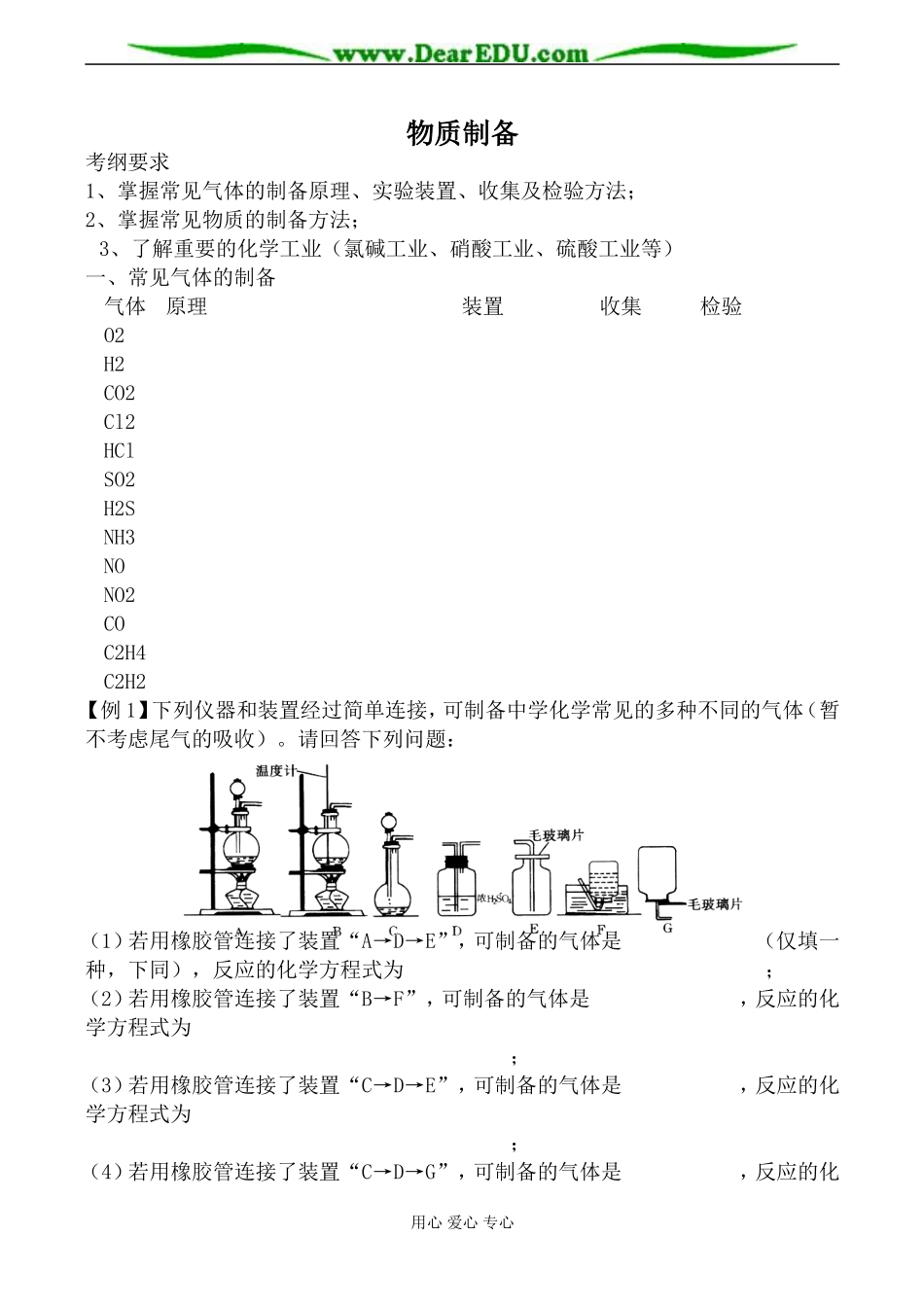
物质制备考纲要求1、掌握常见气体的制备原理、实验装置、收集及检验方法;2、掌握常见物质的制备方法;3、了解重要的化学工业(氯碱工业、硝酸工业、硫酸工业等)一、常见气体的制备气体原理装置收集检验O2H2CO2Cl2HClSO2H2SNH3NONO2COC2H4C2H2【例1】下列仪器和装置经过简单连接,可制备中学化学常见的多种不同的气体(暂不考虑尾气的吸收)。请回答下列问题:(1)若用橡胶管连接了装置“A→D→E”,可制备的气体是(仅填一种,下同),反应的化学方程式为;(2)若用橡胶管连接了装置“B→F”,可制备的气体是,反应的化学方程式为;(3)若用橡胶管连接了装置“C→D→E”,可制备的气体是,反应的化学方程式为;(4)若用橡胶管连接了装置“C→D→G”,可制备的气体是,反应的化用心爱心专心学方程式为。二、其他常见无机物质的制备(如FeSO4·7H2O、纯碱、烧碱、NH3、HNO3、H2SO4、Fe(OH)3胶体,AgI胶体等)【例2】以铜、硝酸、硝酸银、水、空气等为原料,可用多种方法制取Cu(NO3)2。(1)试设计四种制取Cu(NO3)2的途径(用化学方程式表示)①②③④(2)从“绿色化学”的角度(环境保护和经济效益)考虑,大量制取Cu(NO3)2最宜采用上述哪种方法并说明原因。三、典型有机物质的制备(如乙酸乙酯、硝基苯等)【例3】久置的乙醛水溶液会产生分层现象,上层为无色油状液体,下层为水溶液。据测定,上层物质为乙醛的环状聚合物(C2H4O)n,它的沸点比水的沸点高,分子中无醛基,乙醛的沸点是20.8℃,它在溶液中易被氧化,氧化产物的沸点是117.9℃,从久置的乙醛水溶液中提取乙醛(仍得到乙醛水溶液),可利用如下反应:(C2H4O)nnC2H4O;△H<0。试回答下列问题:(1)先分离混合物得到(C2H4O)n,基本方法是:将混合物放入分液漏斗中,静置分层后,打开活塞,将下层液体放入烧杯中,然后。(2)设计一简单实验证明久置的乙醛是否被氧化(写出简要操作步骤、使用的试剂、实验现象和结论)。(3)当n=3时,试写出(C2H4O)n的结构简式(4)提取乙醛的装置如图,烧瓶中的液体是(C2H4O)n和6mol·L—1H2SO4的混合物,锥形瓶中盛放蒸馏水,加热混合物至沸腾,(C2H4O)n缓缓分解,生成的气体导入锥形瓶中。①冷凝管中冷凝水的进口是(填“a”或“b”)。②若实验过程中不使用冷凝管冷却,随着蒸发的进行,溶液中有黑色物质和刺激性气味气体生成。请用化学方程式表示这一现象:。③当锥形瓶内导管口气泡越来越少时,表明乙醛基本部分蒸出,实验结束,拆除实验装置的第一步操作是。用心爱心专心H+