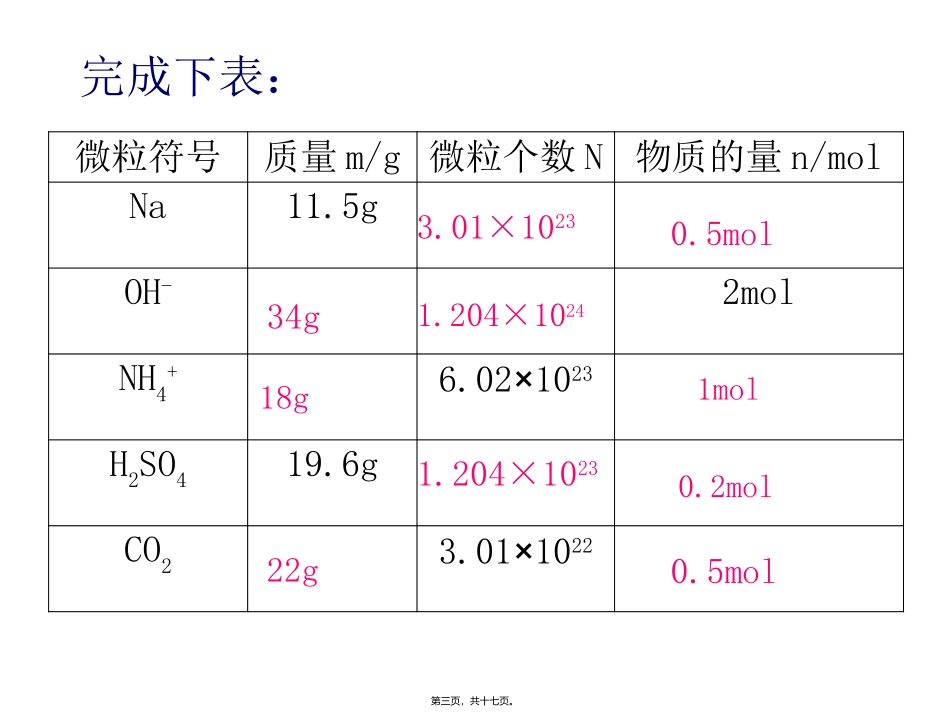
高二化学组课题2物质的量第一页,共十七页。1、了解物质的量的含义及单位摩尔2、了解阿伏伽德罗常数的含义3、了解物质的量、摩尔质量、物质的微粒数、物质的量、气体摩尔体积、物质的量浓度等物理量的含义和它们之间的关系,能用它们进行简单的化学计算直击考点第二页,共十七页。微粒符号质量m/g微粒个数N物质的量n/molNa11.5gOH-2molNH4+6.02×1023H2SO419.6gCO23.01×1022完成下表:3.01×10231.204×10241.204×102334g18g22g0.5mol1mol0.2mol0.5mol第三页,共十七页。知识梳理:1.什么是物质的量?他如何表示?它的单位是什么?2.什么是阿伏伽德罗常数?如何表示?3.什么是气体摩尔体积?它在使用时,需要注意什么?4.什么是摩尔质量?摩尔质量与相对分子质量有什么关系?5.欲用58.5gNaCl配置浓度为1mol/L的溶液,应如何操作?需要注意什么问题?6.请用图示法画出物质的量(n)与质量(m)、气体体积(V)、溶液的物质的量浓度(C)之间的转化关系。第四页,共十七页。一、物质的量和摩尔质量1.物质的量是一个物理量,其意义是表示含有一定量数目的_________的集体,符号为______,______是物质的量的单位(国际单位制的7个基本单位之一)。2.1mol任何粒子集体所含的粒子数与0.012kg12C中所含的碳原子数相同,约为____________,叫做____________常数,符号为______。计算公式为n=______。微观粒子n摩尔6.02×1023阿伏加德罗NANNA第五页,共十七页。例1、下列说法正确的是()A.摩尔是国际单位制中七个基本物理量之一B.物质的量是把物质的质量和微观粒子数联系起来的一个基本物理量C.1mol任何物质的质量就是该物质的相对分子质量D.阿伏伽德罗常数个H2所含分子的物质的量为1molD第六页,共十七页。3.单位物质的量的物质所具有的质量叫做__________,它的常用单位为____________。物质的摩尔质量在数值上等于其_______________________________。计算公式为n=______。摩尔质量g/mol相对原子质量或相对分子质量mM例3、下列正确的是()A.摩尔可以把物质的宏观数量(质量、气体体积等)与微观粒子的数量联系起来B.水的摩尔质量和1mol水的质量均可计为18g·mol-1C.水的摩尔质量和1mol水的质量均可计为18gD.硫酸和磷酸的摩尔质量在数值上相等D第七页,共十七页。二、气体摩尔体积1.单位物质的量的气体所占的体积叫做____________,表示为______。计算公式为气体的摩尔体积=_______________,2.标准状况是指____________℃、1.01×105Pa的状态,此时,气体摩尔体积约为____________L/mol。3.阿伏加德罗定律是指在相同温度和压强下,同体积的任何____________体都含有相同数目的分子。同温同压时,气体的体积之比等于____________之比。即Vm=Vn;常用单位有____________和____________。气体摩尔体积Vm气体所占的体积气体的物质的量L/molm3/mol022.4气物质的量第八页,共十七页。例4、设NA表示阿伏加德罗常数的值,下列说法正确的是()A.在标准状况下,以任意比例混合的CH4与CO2混合物22.4L,所含有的分子数为NAB.在标准状况下,NA个水分子所占的体积为22.4LC.22.4LH2所的H2分子数为NAD.常温常压下,28克氮气含有的核外电子数为10NAA第九页,共十七页。三、物质的量浓度1.物质的量浓度是以____________里所含溶质的物质的量来表示溶液组成的物理量。其单位是____________,计算公式为____________。2.配制一定物质的量浓度溶液的步骤。____________、____________(或量取)、__________(或稀释)、冷却至室温、____________、洗涤、____________、定容、摇匀、装瓶贴标签。单位体积mol/LcB=nBV计算称量溶解转移振荡第十页,共十七页。设NA代表阿伏加德罗常数,下列说法是否正确?①1mol任何物质中都含有6.02×1023个粒子;②96g氧的物质的量为3mol;③常温常压下,48g臭氧中含有的氧原子数为3NA;④在铁和足量的氯气的反应中,1mol铁失去的电子数为3NA;⑤1.8gD2O中含有NA个中子;(实验班选做)⑥1L1mol/L的盐酸溶液中,所含氯化氢分子数为NA;(实验班选做)⑦常温常压下,1mol氦气含有的原子数为2NA;⑧12g碳单质中所含碳原子的数目叫做阿伏加德罗常数典型例题例2第十...