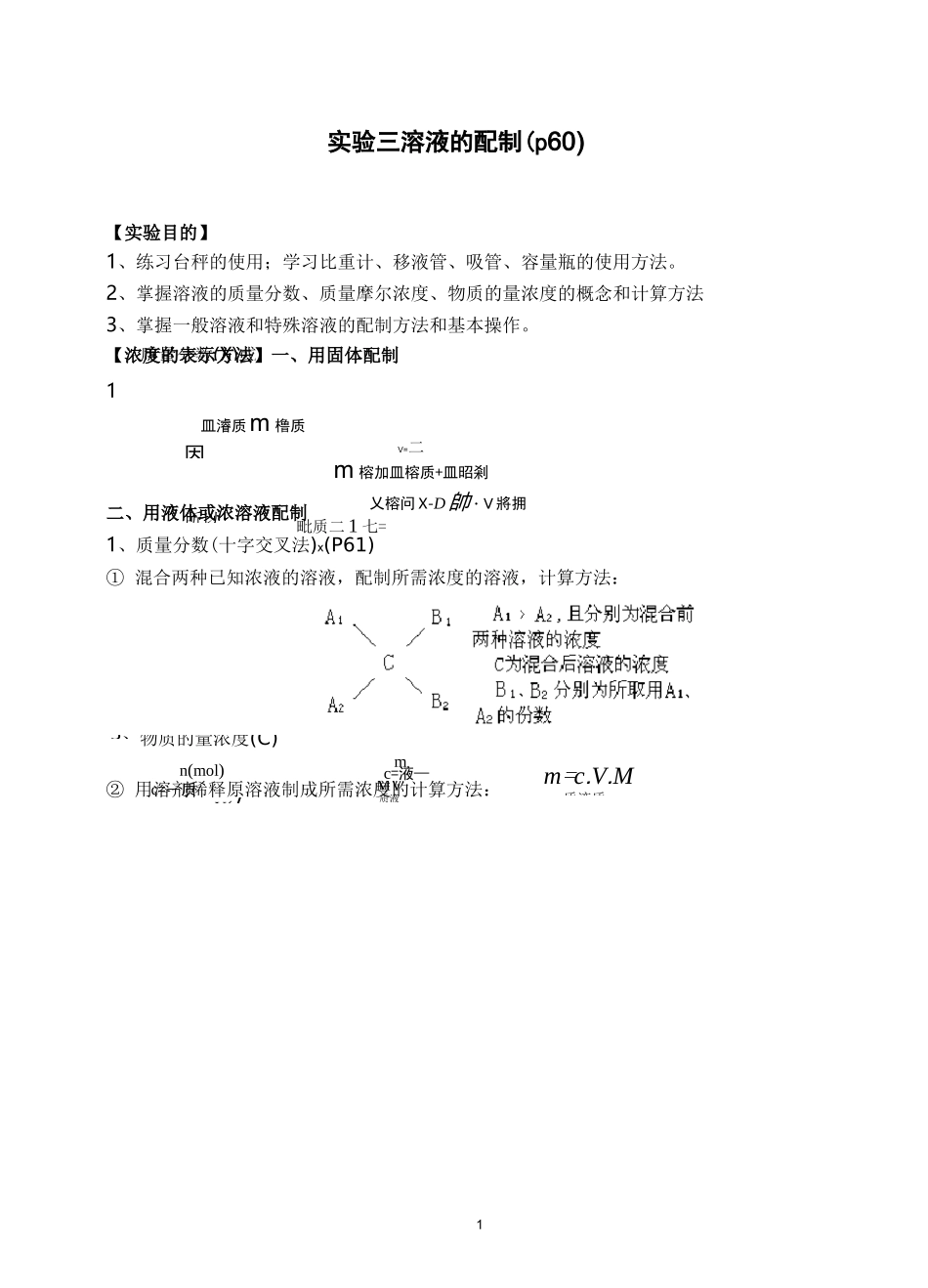
1质量分数(X)或因所以:乂榕问X-D帥・V將拥毗质二1七=2、如落剂为水’质量摩尔浓度(m或3、n(mol)b=溶质溶剂质量(kg)物质的量浓度(C)n(mol)c=―质V(LM-b■M-b-P加■V朋皿橹厭二二mc=液—MV质液100100m=c
M质液质实验三溶液的配制(p60)【实验目的】1、练习台秤的使用;学习比重计、移液管、吸管、容量瓶的使用方法
2、掌握溶液的质量分数、质量摩尔浓度、物质的量浓度的概念和计算方法3、掌握一般溶液和特殊溶液的配制方法和基本操作
【浓度的表示方法】一、用固体配制1皿濬质m橹质V=二m榕加皿榕质+皿昭剎二、用液体或浓溶液配制1、质量分数(十字交叉法)x(P61)①混合两种已知浓液的溶液,配制所需浓度的溶液,计算方法:②用溶剂稀释原溶液制成所需浓度的计算方法:B及所加水的份2、物质的量浓度(c)由已知物质的量浓度溶液稀注:市售浓H2SO4c=18
L-1浓H3PO4c=14
L-1浓HAcc=17
L-1【配制方法】1、粗略配制(性质实验):仪器:台秤(称固体)、量筒、量杯、烧浓HC1浓HNO3c=12mol
L-1c=16mol
L-1c=14
L-1搅棒、比重计
2c为混台后溶液的浓度分别为所取用山的份数配制时应先加水或稀溶液,然后加浓溶液
搅动均匀,将溶液转移到试剂瓶中,贴上标签,备用
计算固体试剂的质量或液体试剂的体积;b•用台称称量固体试剂或用量筒量取液体试剂;c•在烧杯中溶解,并稀释至刻度或直接稀释至刻度
注意:如果溶液放热,需冷却至室温后,再用水稀释至刻度
搅动使其均匀,然后移入试剂瓶中,贴上标签备用
2、准确配制(定量测定)仪器:分析天平、吸量管、移液管、容量瓶步骤:a•计算固体试剂的质量或液体试剂的体积b•用分析天平称量固体试剂或用吸量管量取液体试剂;c•在烧杯中用