m干煤装装FH:M(r据的选收专题讲座二气体的实验室制备、净化和收集■知识梳理1
气体制备实验的基本思路2
重要气体的发生装置依据制备气体所需的反应物状态和反应条件,可将制备气体的发生装置分为三类:(1)固体+固体一△一气体发生装置:制备气体:O2、NH3、CH4等
(2)固体+液体或液体+液体一△-气体发生装置:制备气体:Cl2、C2H4等
(3)固体+液体(不加热)一气体发生装置:制备气体:选择合适的药品和装置能制取中学化学中常见的气体
枚集通过顺斜Y形许絶鍍悴与固体捲触发半
反应,控制反应的±iryW||3
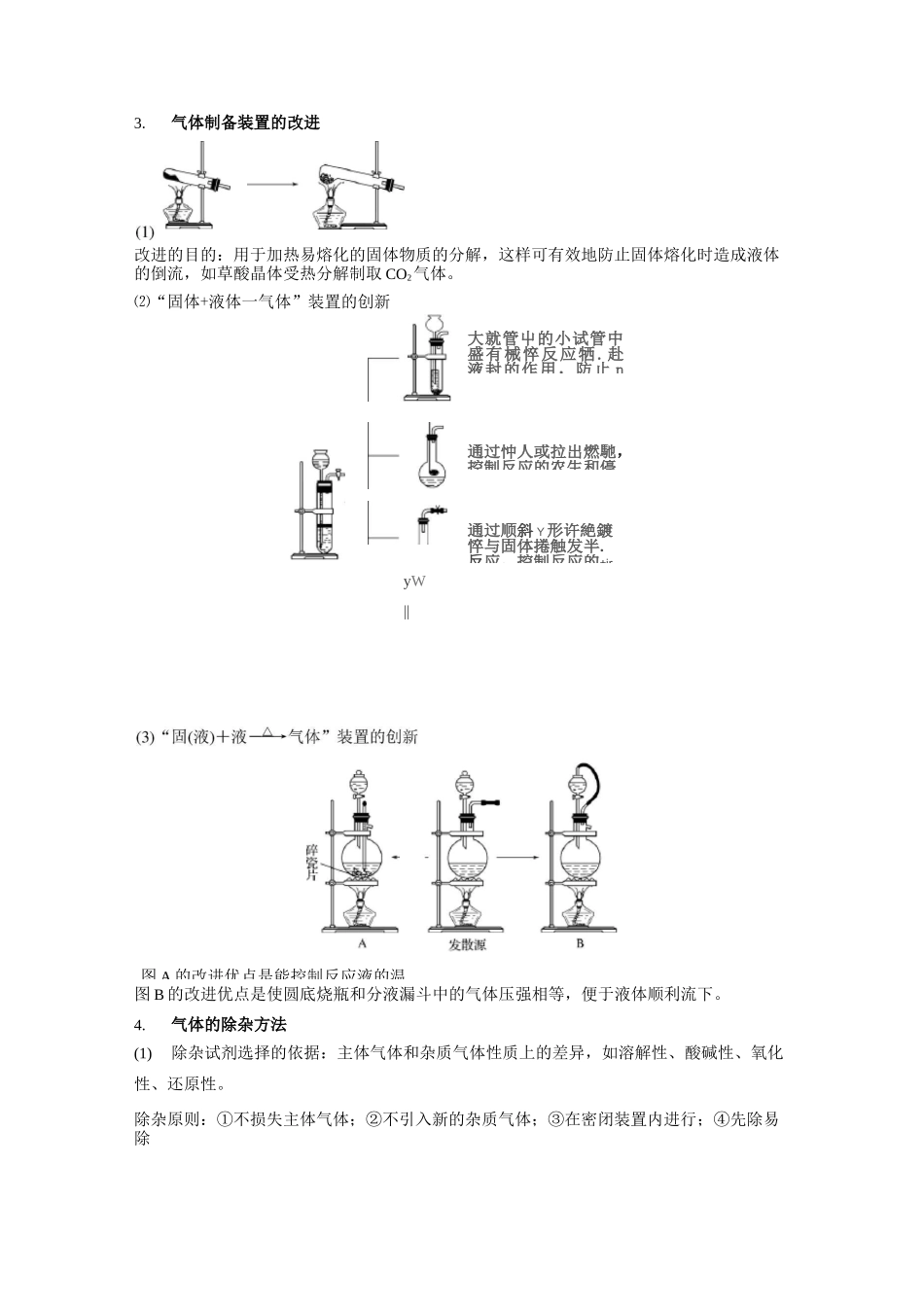
气体制备装置的改进改进的目的:用于加热易熔化的固体物质的分解,这样可有效地防止固体熔化时造成液体的倒流,如草酸晶体受热分解制取CO2气体
⑵“固体+液体一气体”装置的创新图B的改进优点是使圆底烧瓶和分液漏斗中的气体压强相等,便于液体顺利流下
气体的除杂方法(1)除杂试剂选择的依据:主体气体和杂质气体性质上的差异,如溶解性、酸碱性、氧化性、还原性
除杂原则:①不损失主体气体;②不引入新的杂质气体;③在密闭装置内进行;④先除易除大就管屮的小试管中盛有械悴反应牺
赴液封的作用,防止n通过忡人或拉出燃馳,控制反应的农生和停图A的改进优点是能控制反应液的温类液态干燥固态干燥固态干燥固体,加装常见干燥I浓H2SO4(酸性、化无水氯化钙(中III碱石灰(碱除杂试剂Cu、排气收集方排水向上排空气向下排空气收集气体的类于水,又不与水应的气密度大于空气不与空气中的分反密度小于空气不与空气中的分反收集可收集的气体(举O2、H2、NO、COci2、SO2、NO2、COH2、NH3(in的杂质气体
(2)气体干燥净化装置当CO2中混有O2杂质时,应选用上述I〜W中的w装置除O2,除杂试剂是Cu粉
气体的收集方法6•集气装置的创新——排液集气装置装置(I)从a管进气b管出水可收集难溶