第一章气体的pVT性质1
1物质的体膨胀系数与等温压缩率的定义如下试推出理想气体的,与压力、温度的关系
解:根据理想气体方程1
20℃,101
325kPa的条件常称为气体的标准状况,试求甲烷在标准状况下的密度
解:将甲烷(Mw=16
042g/mol)看成理想气体:PV=nRT,PV=mRT/Mw甲烷在标准状况下的密度为=m/V=PMw/RT=101
32516
3145273
15(kg/m3)=0
716kg/m31
3一抽成真空的球形容器,质量为25
0000g充以4℃水之后,总质量为125
若改充以25℃,13
33kPa的某碳氢化合物气体,则总质量为25
试估算该气体的摩尔质量
水的密度1g·cm3计算
解:球形容器的体积为V=(125-25)g/1g
cm-3=100cm3将某碳氢化合物看成理想气体:PV=nRT,PV=mRT/MwMw=mRT/PV=(25
0163-25
0000)×8
314×298
15/(13330×100×10-6)Mw=30
31(g/mol)1
4两个容积均为V的玻璃球泡之间用细管连结,泡内密封着标准状态下的空气
若将其中的一个球加热到100℃,另一个球则维持0℃,忽略连接细管中气体体积,试求该容器内空气的压力
解:由题给条件知,(1)系统物质总量恒定;(2)两球中压力维持相同
标准状态:因此,1
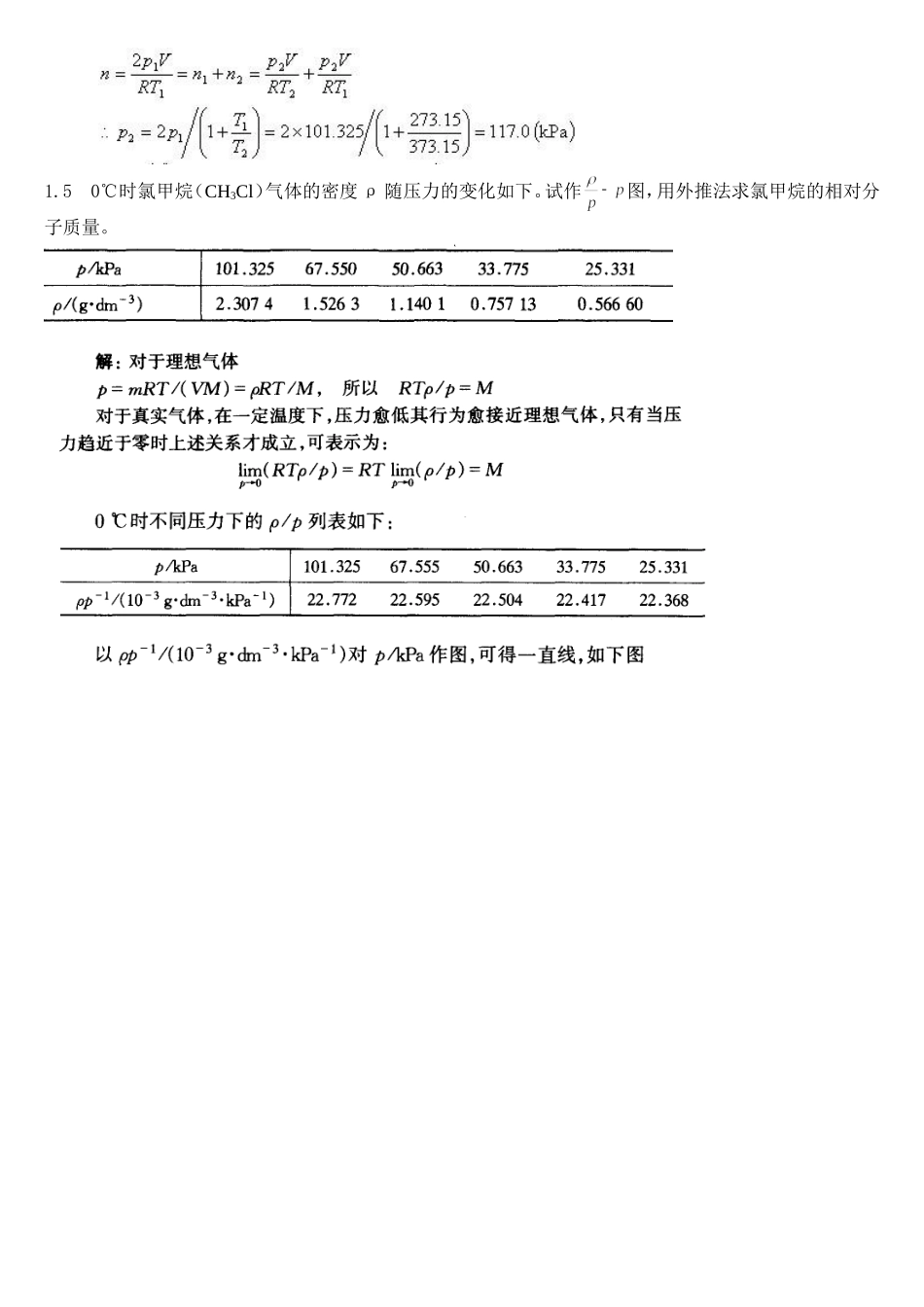
50℃时氯甲烷(CH3Cl)气体的密度ρ随压力的变化如下
试作图,用外推法求氯甲烷的相对分子质量
6今有20℃的乙烷-丁烷混合气体,充入一抽成真空的200cm3容器中,直至压力达101
325kPa,测得容器中混合气体的质量为0
试求该混合气体中两种组分的摩尔分数及分压力
解:将乙烷(Mw=30g/mol,y1),丁烷(Mw=58g/mol,y2)看成是理想气体:PV=nRTn=