高中化学精品备考、学习资料第四节配合物与超分子〖核心素养发展目标〗1
能从微观角度理解配位键的形成条件和表示方法,能判断常见的配合物
能利用配合物的性质去推测配合物的组成,从而形成“结构决定性质”的认知模型
了解超分子的结构特点与性质
一、配合物1.配位键(1)概念:由一个原子单方面提供孤电子对,而另一个原子提供空轨道而形成的化学键,即“电子对给予—接受”键
(2)表示方法:配位键常用A—B表示,其中A是提供孤电子对的原子,叫给予体,B是接受孤电子对的原子,叫接受体
如:H3O的结构式为(3)形成条件+;NH4的结构式为+
形成配位键的一方(如A)是能够提供孤电子对的原子,另一方(如B)是具有能够接受孤电子对的空轨道的原子
①孤电子对:分子或离子中,没有跟其他原子共用的电子对就是孤电子对
如、、分子中中心原子分别有1、2、3对孤电子对
含有孤电子对的微粒:分---子如CO、NH3、H2O等,离子如Cl、CN、NO2等
②含有空轨道的微粒:过渡金属的原子或离子
一般来说,多数过渡金属的原子或离子形成配位键的数目基本上是固定的,如Ag形成2个配位键,Cu2形成4个配位键等
2.配合物(1)概念通常把金属离子或原子(称为中心离子或原子)与某些分子或离子(称为配体或配位体)以配位键结合形成的化合物称为配位化合物,简称配合物
如〖Cu(NH3)4〗SO4、〖Ag(NH3)2〗OH等均为配合物
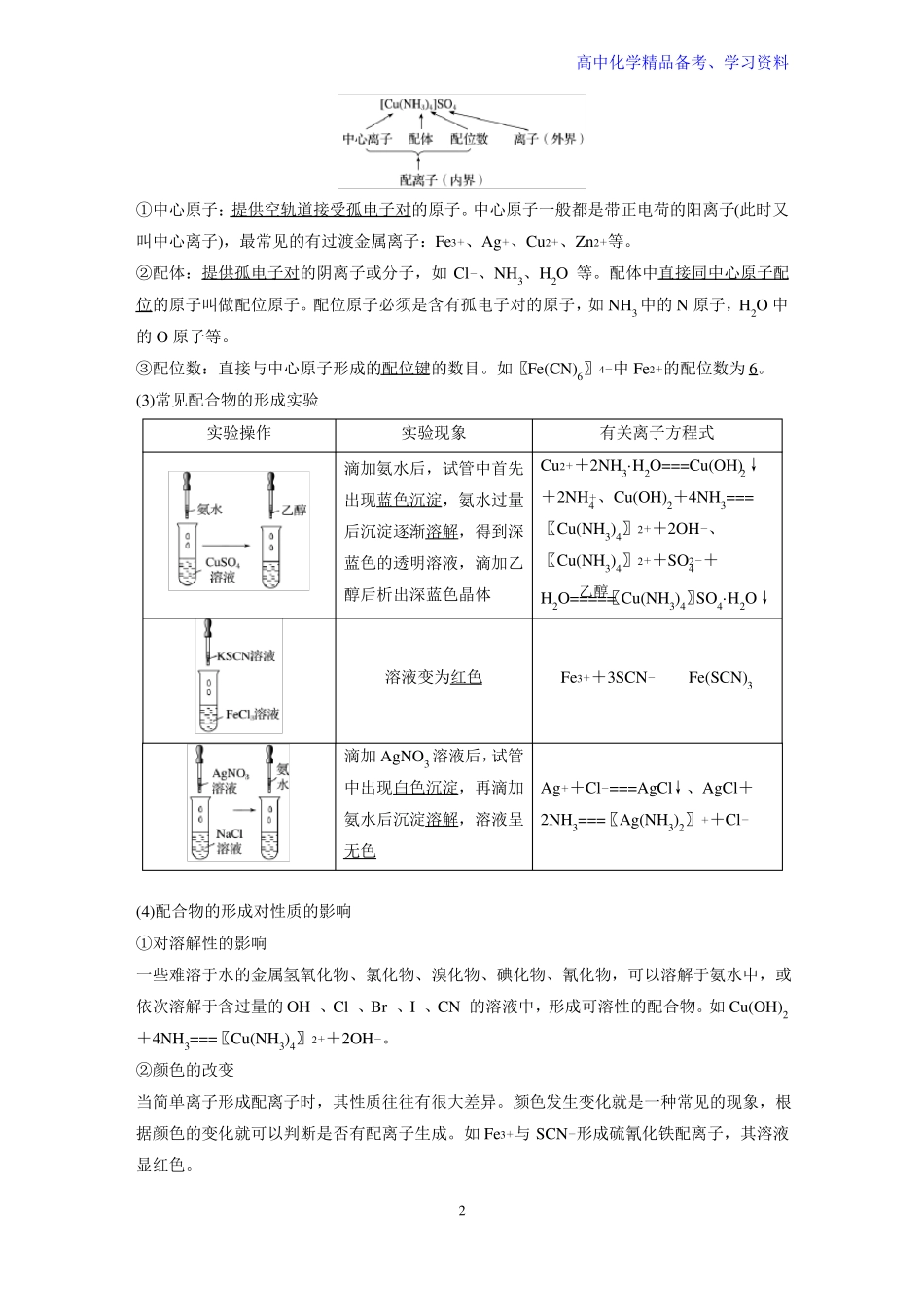
(2)组成配合物〖Cu(NH3)4〗SO4的组成如下图所示:1++高中化学精品备考、学习资料①中心原子:提供空轨道接受孤电子对的原子
中心原子一般都是带正电荷的阳离子(此时又叫中心离子),最常见的有过渡金属离子:Fe3、Ag、Cu2、Zn2等
②配体:提供孤电子对的阴离子或分子,如Cl、NH3、H2O等
配体中直接同中心原子配位的原子叫做配位原子
配位原子必须是含有孤电子对的原子,如NH