8球蛋白的折叠依赖于各种相互作用A
疏水相互作用是蛋白质折叠的主要驱动力蛋白质中的疏水基团彼此靠近、聚集以避开水的现象称之疏水相互作用或疏水效应
氢键和范德华力也是稳定球蛋白的力除了稳定-螺旋和-折叠结构的氢键以外,在多肽链骨架和水之间,多肽链骨架和极性侧链之间,两个极性侧链之间以及极性侧链和水之间也可以形成氢键
大多数氢键都是N-H……O类型的
范德华力包括吸引力和斥力两种相互作用,范德华力只有当两个非极性残基之间处于一定距离时才能达到最大
共价交联和离子相互作用有时有助于球蛋白的稳定共价交联,例如二硫键也有助于某些球蛋白的天然构象的稳定
带有相反电荷的侧链之间的离子相互作用也能帮助稳定球蛋白,虽然这种作用很弱
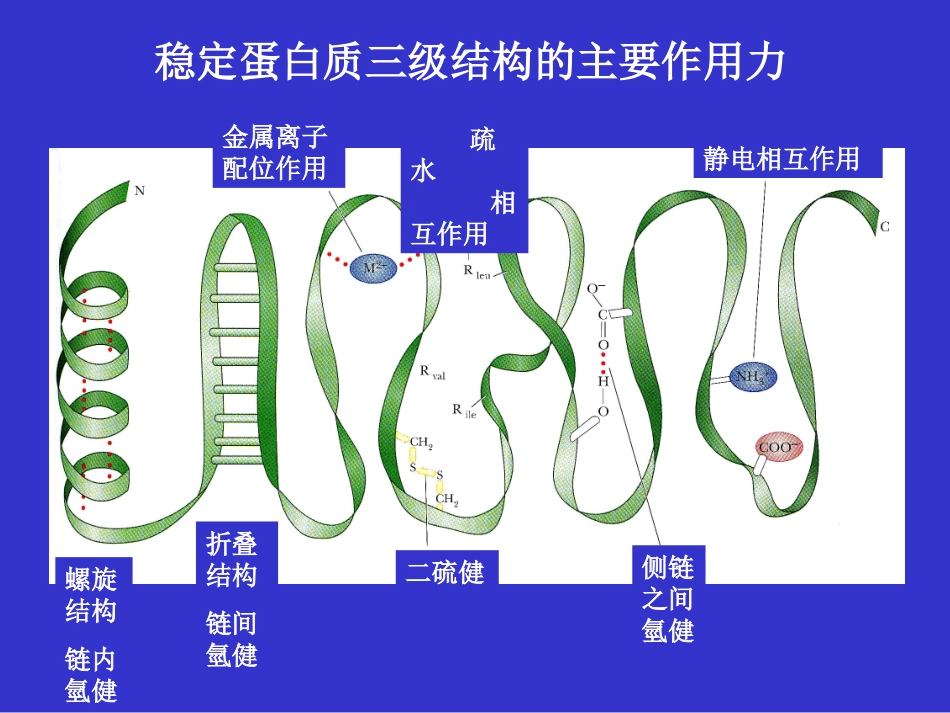
疏水相互作用静电相互作用金属离子配位作用折叠结构链间氫健螺旋结构链内氫健二硫健侧链之间氫健稳定蛋白质三级结构的主要作用力4
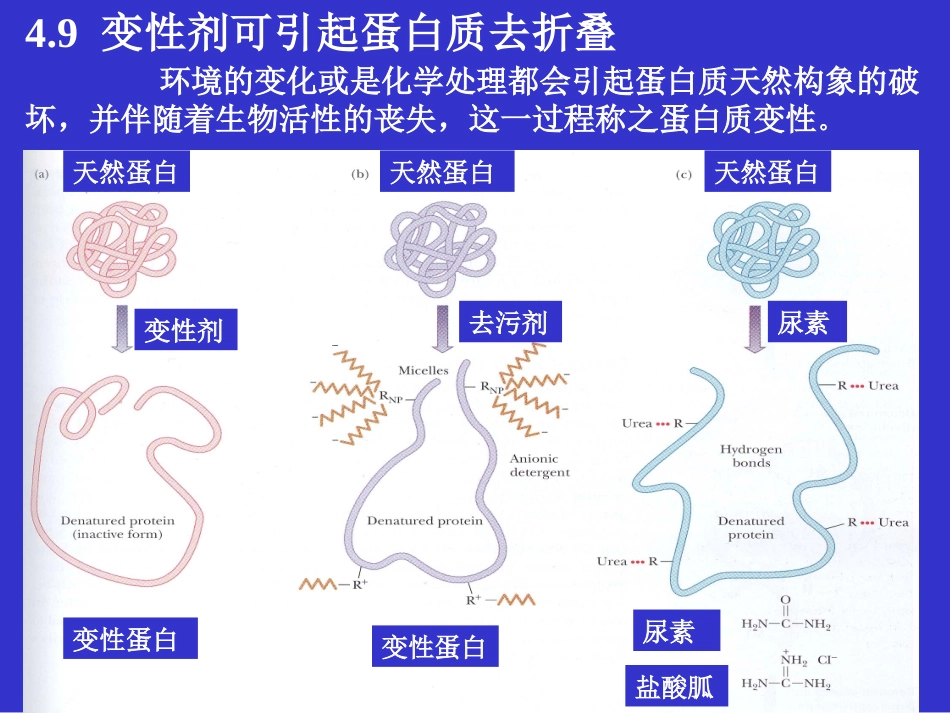
9变性剂可引起蛋白质去折叠环境的变化或是化学处理都会引起蛋白质天然构象的破坏,并伴随着生物活性的丧失,这一过程称之蛋白质变性
变性剂天然蛋白天然蛋白天然蛋白去污剂尿素变性蛋白变性蛋白尿素盐酸胍核糖核酸酶A变性,酶的三级结构和活性完全丧失,生成含有8个巯基的多肽链
加脲和巯基乙醇去除脲和巯基乙醇,又恢复到天然状态核糖核酸酶A变性和复性Anfinsen等人用含有2-巯基乙醇的8M脲的变性剂使核糖核酸酶A(RnaseA)变性,导致酶的三级结构和催化活性完全丧失,生成含有8个巯基的多肽链
如果使变性的酶氧化和再折叠,8对巯基可以随机配对的话,那么就有可能生成105种二硫键不同的结构,但具有生物活性的只有一种
事实上当除去还原剂后,在8M脲的环境下氧化,形成的蛋白质中有99%都含有不正确的二硫键,而且活性大约是原来酶活性的1%
如果将还原剂和脲同时都除去,并且稀释还原的蛋白和将它于生理pH条件下暴露在空气中,RnaseA会自发地获得它的