24/12/2621:05第一章原子结构和元素周期性1-1原子结构理论的发展概况1-2量子力学的原子模型1-3核外电子排布与元素周期表1-4原子性质的周期性24/12/2621:051-1原子结构理论的发展概况1-1-1原子的含核模型1911年,英国物理学家卢瑟福,α粒子散射实验原子的中心有一个带正电的原子核,电子在它的周围旋转
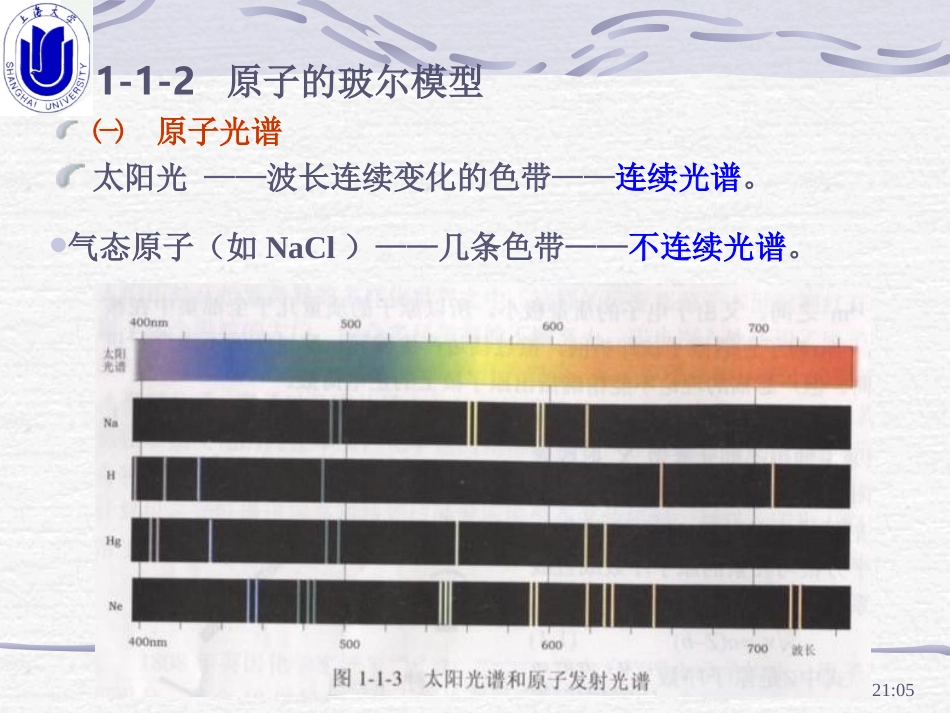
原子的直径10-10m电子的直径10-15m原子核的直径10-16m~10-14m24/12/2621:051-1-2原子的玻尔模型㈠原子光谱太阳光——波长连续变化的色带——连续光谱
气态原子(如NaCl)——几条色带——不连续光谱
24/12/2621:05㈡氢原子光谱氢原子光谱是最简单的一种原子光谱,对它的研究也比较详尽
氢原子光谱实验如图所示,氢原子光谱在可见光区有四条比较明显的谱线,如图,通常用HαHβHγHδ来标志
这个光谱系叫Balmer系
)n121(B22在一个熔接着两个两极,且抽成高真空的玻璃管内,装进高纯的低压氢气,然后,在两极上施加很高的电压,使低压氢气放电,氢原子在电场的激发下发光,若使这种光线经狭缝,再通过棱镜分光后,可得含有几条谱线的线状光谱——氢原子光谱
24/12/2621:051913年玻尔(N
Bohr)在普朗克的量子论(1900)、爱因斯坦的光子学说(1905)和卢瑟福的有核原子模型(1911)的基础上,提出了原子结构理论的三点假设
㈢玻尔的氢原子模型⑴定态假设⑵频率公式⑶量子化规则电子绕核旋转,作圆周运动,在一定轨道上运动的电子具有一定的能量,称为“稳定状态”
简称“定态”
电子在定态轨道上运动,并不辐射能量
能量最低的定态称“基态”,其他的定态称为“激发态”
原子中电子可以由一定态跳到另一定态,在此过程中放出或吸收辐射,其频率ν则由下式决定:ΔE=hυ=E2-E1(E2>E1)上式称为Bohr频率公