利用气体混合物中各组分在液体溶剂中溶解度的差异来分离气体混合物的操作称为吸收
溶质A惰性组分B吸收剂S什么是吸收
AA+BS(气体)(液体)第4章气体吸收1、吸收的目的和依据目的:(1)回收有用物质;(2)脱除有害成分
依据:混合气体中各组分在某种溶剂中溶解度的差异
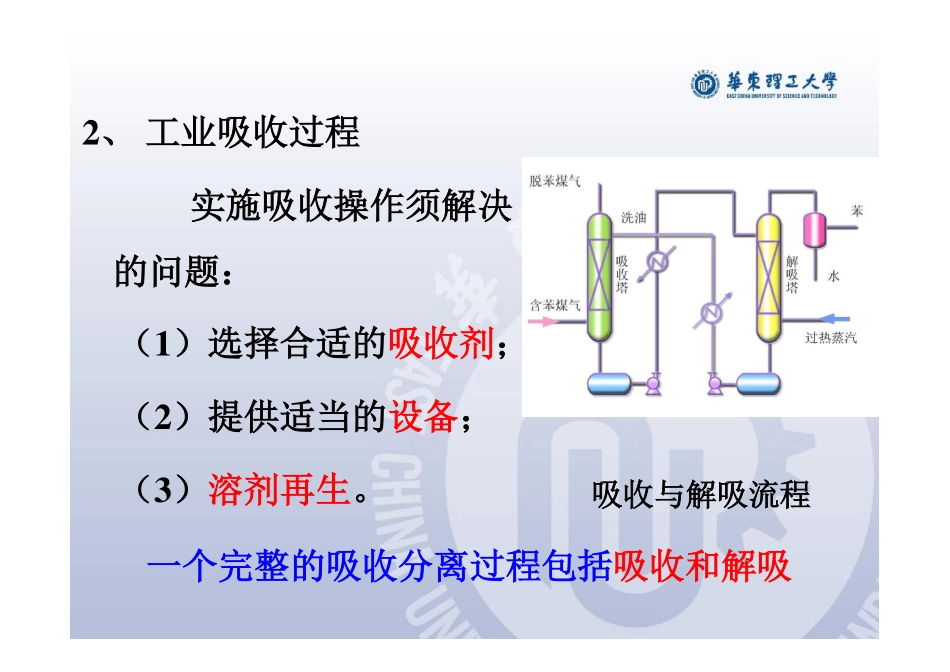
1概述一个完整的吸收分离过程包括吸收和解吸2、工业吸收过程实施吸收操作须解决的问题:(1)选择合适的吸收剂;(2)提供适当的设备;(3)溶剂再生
吸收与解吸流程技术要求:溶解度大;选择性高;对温度的敏感性强,易解吸
经济及安全要求:蒸汽压要低,不易挥发;较好的化学稳定性;黏度小;价廉,易得,无毒,不易燃易爆
3、溶剂的选择物理吸收:气体各组分因在溶剂中溶解度的不同而被分离的吸收操作
化学吸收:利用化学反应而实现吸收的操作
化学吸收应满足的条件:(1)反应的可逆性;(2)较高的反应速率
4、气体吸收的分类吸收的操作费用:(1)流动能耗;(2)溶剂损耗;(3)解吸操作费用(此项费用最大)
5、吸收操作的经济特性常用的解吸方法:升温、减压、吹气,升温和吹气通常同时进行
l升温、减压→溶质的溶解度降低,→有利于溶质的析出→溶液浓度降低l通过吹气→将溶质随气体一起带出,完成解吸过程
解吸目的:降低溶液浓度6、气液两相的接触方式级式接触微分接触气液传质设备7、本章基本假定(1)气体中只有一个组分溶于溶剂中,其余可作为惰性组分
(2)溶剂蒸气压很低,气体中不含溶剂蒸气
•因此,y代表气相•x代表液相
•x,y为同一种物质4
2气液相平衡吸收与传热的比较过程传递对象推动力极限传热热量T-t温度相等吸收物质y-x
两相浓度相等
原因:气液相平衡不同于冷热流体之间的热平衡
相界面水pG气相主体pi液相主体传质方向CiCL空气+氨气吸收--------相际间传质的最终状态相平衡与热平衡不同之处:▲达到相平衡时,一般两相浓度不相等