第第3333课时课时水的电离和溶液的酸碱性水的电离和溶液的酸碱性第八章水溶液中的离子平衡一、水的电离1
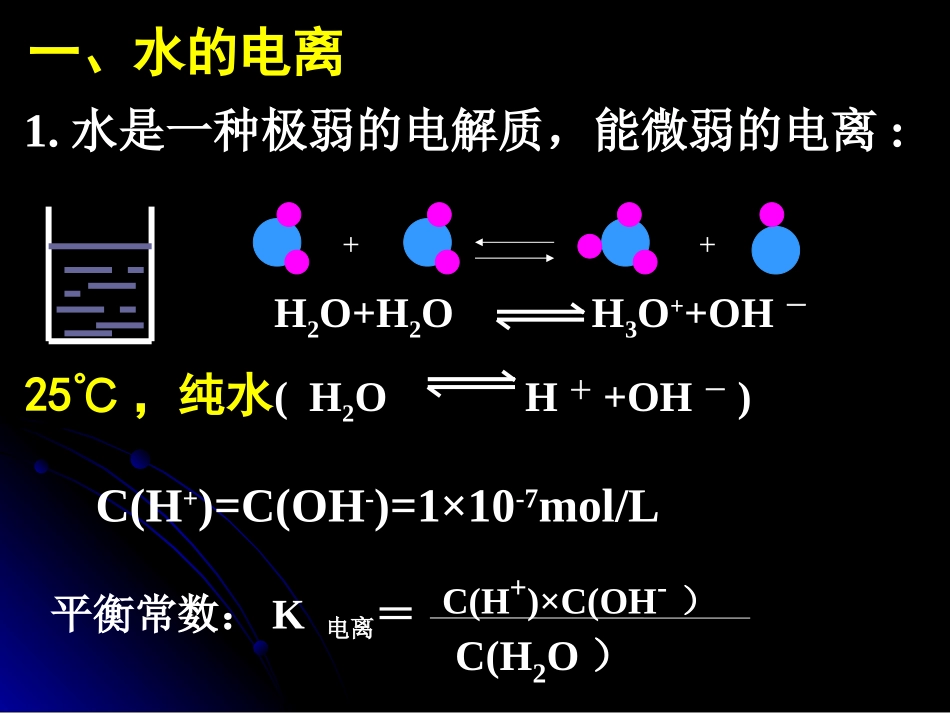
水是一种极弱的电解质,能微弱的电离:25℃,纯水++H2O+H2OH3O++OH-(H2OH++OH-)C(H+)=C(OH-)=1×10-7mol/L平衡常数:K电离=C(H+)×C(OH-)C(H2O)在一定温度时:C(H+)×C(OH-)=Kw,叫水的离子积25℃时,Kw=1×10-142、水的离子积水的浓度为常数,所以KW=C(H+)×C(OH-)提问:水的离子积会受什么外界条件影响
3、影响水电离的因素(1)加入酸或碱,抑制水的电离,Kw不变;(2)电离过程是一个吸热过程,升高温度,促进水的电离,水的离子积增大
如:在100℃时,KW=1×10-12
④根据Kw=C(H+)×C(OH-)在特定温度下为定值,C(H+)和C(OH-)可以互求
③不论是在中性溶液还是在酸碱性溶液,水电离出的C(H+)=C(OH-)②常温下,任何稀的水溶液中C(H+)×C(OH-)=1×10-14注意:①任何水溶液中H+和OH-总是同时存在的,只是相对含量不同
二、溶液的酸碱性与pH值pH值计算1——酸的稀释例题:在25℃时,pH值等于3的盐酸溶液稀释到原来的100倍,pH值等于多少
解:pH=-lg[H+]=-lg1
0×10-5=5关键:抓住氢离子浓度进行计算
[H+]==1
0×10-5mol/L2、溶液的pH值---pH=-lg[H+]pH值计算2——碱的稀释例题:在25℃时,pH值等于12的强碱溶液稀释到原来的100倍,pH等于多少
解:稀释前:[OH-]=pH=-lg[H+]关键:抓住氢氧根离子离子进行计算
稀释后:[OH-]=[H+]==10=1×10-2mol/L=1×10-4mol/L==1×10-10mol/L课前练习:溶液稀释的PH计算溶液的稀释溶液的稀释稀释