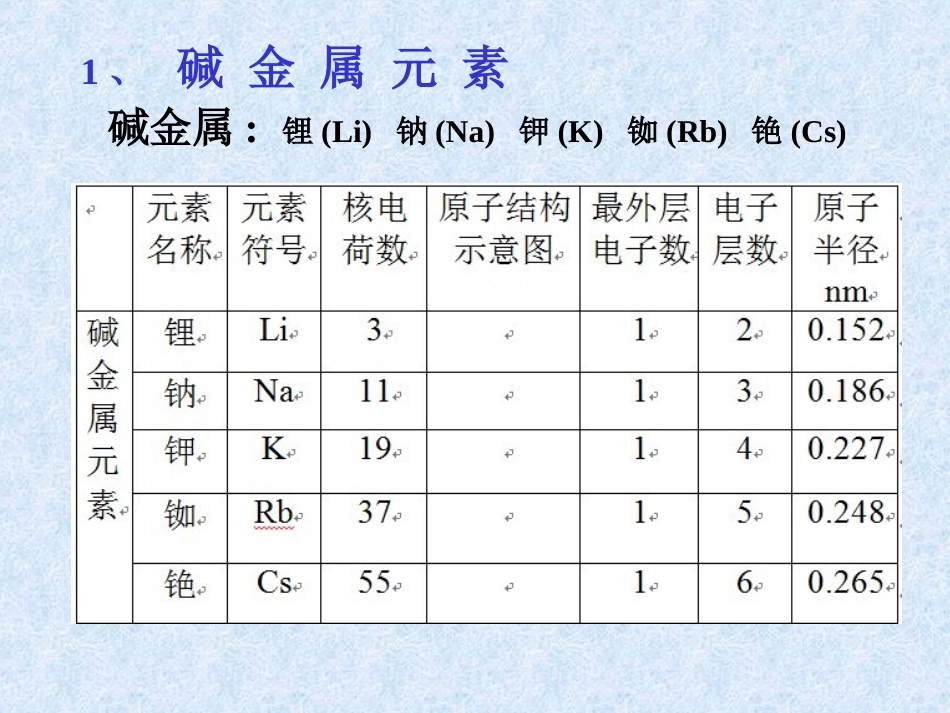
第一章物质结构元素周期律第一节元素周期表第二课时元素的性质与原子结构1、碱金属元素碱金属:锂(Li)钠(Na)钾(K)铷(Rb)铯(Cs)81281818+55812818+378128+19812+11+321Na钠K钾Li锂Rb铷Cs铯碱金属原子结构示意图:最外层电子数均为1个碱金属原子结构异同:异:核电荷数:由小→大;电子层数:由少→多;同:钾在空气中燃烧钾与水反应钠与水反应钠与钾性质对比实验保存于煤油中;用镊子夹取,在玻璃片上小刀切割,滤纸吸干煤油
钾的保存及取用方法:Na与K和水反应方程式:2Na+2H2O=2NaOH+H2↑2K+2H2O=KOH+H2↑1写出锂与稀盐酸反应的离子方程式2
钾与水反应的离子方程式3
过氧化钾与CO24
超氧化钾与水,CO25
氧化锂与水,CO2练习:完成下列方程式:2Li+2H+=2Li++H2↑2K+2H2O=2K++2OHˉ+H2↑2K2O2+2CO2=2K2CO3+O2↑4KO2+2CO2=2K2CO3+3O2↑4KO2+2H2O=4KOH+3O2↑Li2O+H2O=2LiOHLi2O+CO2=Li2CO3LiNaKRbCs1
相似性:1)都易失电子表现强还原性2)化合物中均为+1价总结:碱金属的原子结构2
递变性:核电荷数电子层数(电子层数的影响大于核电荷数的影响)失电子能力还原性金属性原子半径化学性质相似最外层上都只有一个电子核对最外层电子的引力与O2反应反应不如钠剧烈,生成Li2O点燃剧烈燃烧,生成Na2O2燃烧更加剧烈生成比过氧化物复杂的氧化物遇空气立即燃烧,生成更复杂的氧化物遇空气立即燃烧,生成更复杂的氧化物LiNaKRbCs与H2O反应剧烈,生成H2更剧烈,生成H2轻微的爆炸,生成H2遇水立即燃烧,爆炸结论金属性逐渐增强碱金属的化学性质遇水立即燃烧,爆炸碱金属元素的单质的性质:1、与非金属单质的反应:4Li+O2