第1节碳、硅及无机非金属材料[考试说明]1
了解碳、硅单质及其化合物的主要性质及应用
了解碳、硅及其化合物对环境质量的影响
了解常见无机非金属材料的性质和用途
[命题规律]碳、硅及其化合物的性质是高考的常考点,其考查方式有:结合原子结构、元素周期律以选择题型考查碳、硅及其化合物的性质及应用;以新材料、新技术为背景结合工艺流程图以填空题型考查碳、硅及其化合物的性质及应用等
考点1碳、硅单质及其氧化物的性质知识梳理1
碳单质的存在、性质和用途自然界中存在形态□游离态和化合态物理性质金刚石:熔点高,硬度□大,不导电石墨:熔点高,质□软,有滑腻感,能导电活性炭:有疏松多孔的结构,能吸附色素和异味(物理变化)化学性质与O2反应O2充足时:□C+O2=====CO2O2不足时:□2C+O2=====2CO与氧化物反应CuO:□2CuO+C=====2Cu+CO2↑(冶炼金属)SiO2:□SiO2+2C=====Si+2CO↑(制取粗硅)H2O:□C+H2O(g)=====CO+H2(制取水煤气)CO2:C+CO2=====□2CO与强氧化性酸反应浓H2SO4:□C+2H2SO4(浓)=====CO2↑+2SO2↑+2H2O用途金刚石:用作切削刀具、装饰品等石墨:作电极、高温润滑剂、铅笔芯等2.硅单质的存在、性质和制备(1)存在、结构及物理性质(2)化学性质硅的化学性质不活泼,常温下不能被浓硫酸、浓硝酸等强氧化剂氧化,只能与F2、氢氟酸、强碱溶液反应;在加热条件下,能与O2、Cl2等少数非金属单质化合
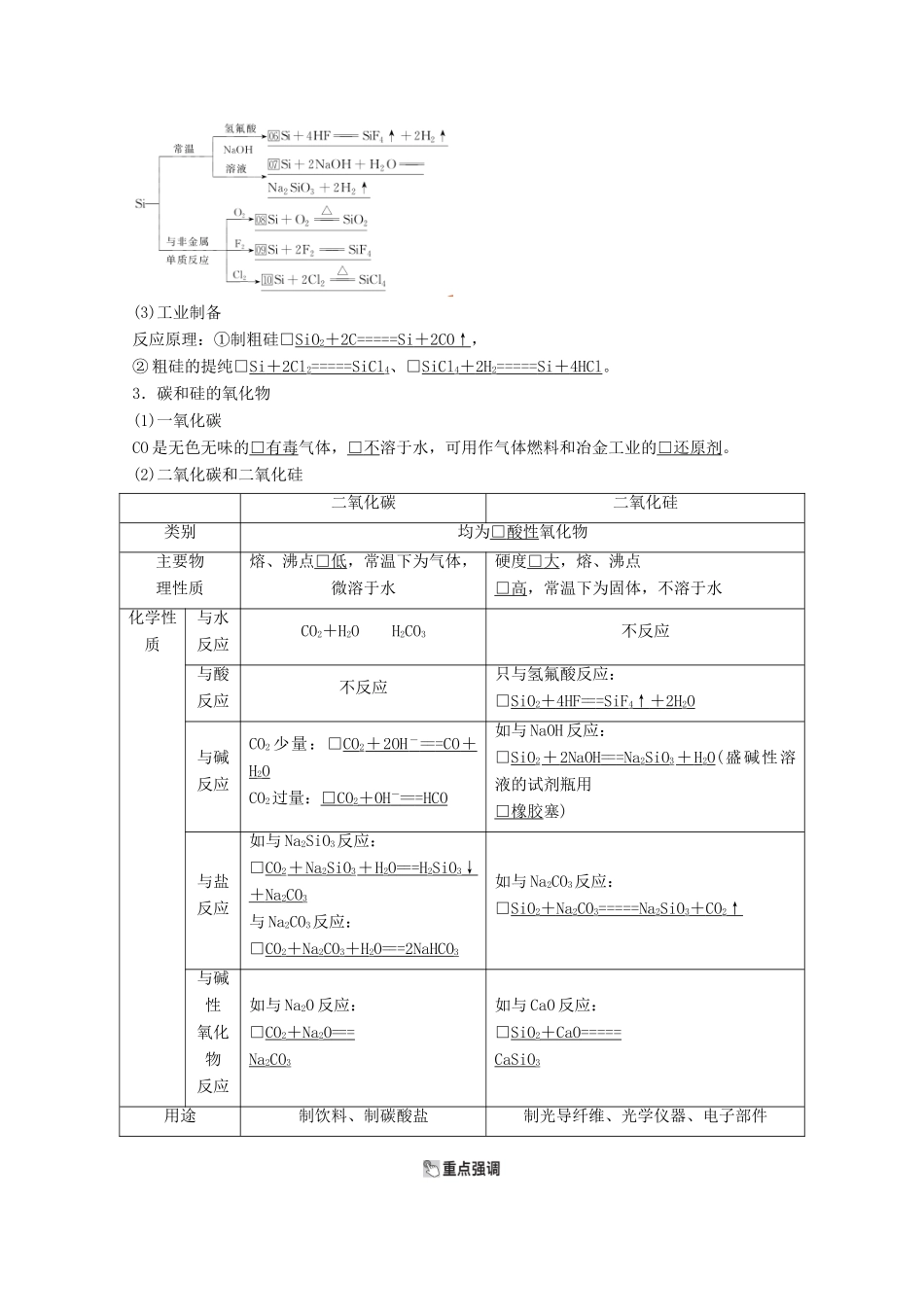
写出下列相关反应的化学方程式:(3)工业制备反应原理:①制粗硅□SiO2+2C=====Si+2CO↑,②粗硅的提纯□Si+2Cl2=====SiCl4、□SiCl4+2H2=====Si+4HCl
3.碳和硅的氧化物(1)一氧化碳CO是无色无味的□有毒气体,□不溶于水,可用作气体