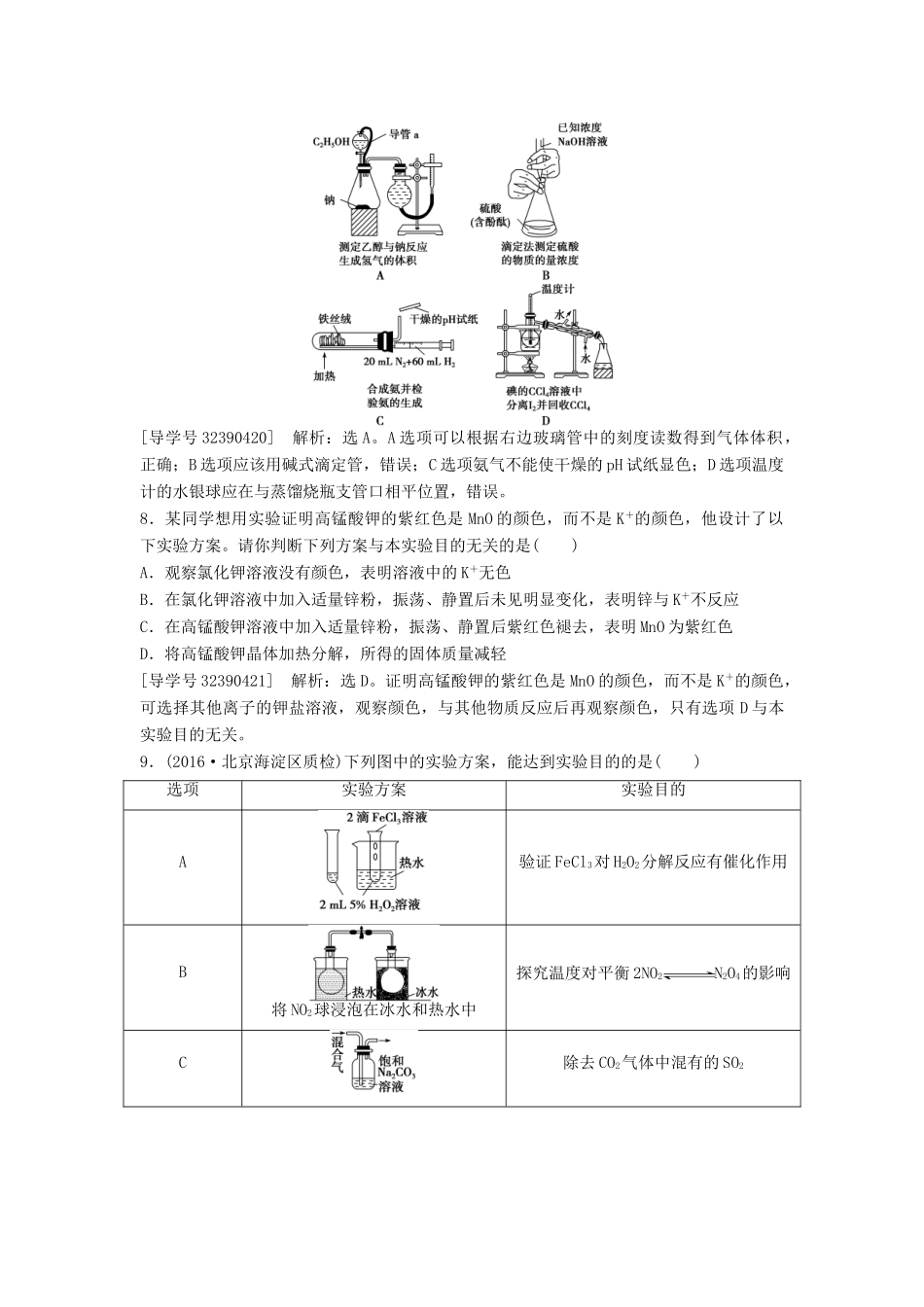
第33讲化学实验设计与评价1.下列实验方案可行的是()A.用1mol/L的盐酸与MnO2反应制取氯气B.用湿润的淀粉碘化钾试纸鉴别二氧化氮和溴蒸气C.用10mL量筒量取8
50mL浓硫酸用于配制一定物质的量浓度的稀硫酸D.用湿润的有色纸条鉴别氯化氢和氯气[导学号32390414]解析:选D
制取氯气需要浓盐酸,而1mol/L的盐酸是稀盐酸,A项错误;二氧化氮与水反应生成的硝酸以及溴蒸气都具有氧化性,都能氧化碘离子,B项错误;量筒属于粗量仪器,不能精确到小数点后两位数,C项错误
某同学设计了如图实验装置探究硝酸的性质,根据图示判断下列结论不正确的是()A.试管内壁上的“黄霜”的成分是硫B.该实验既说明了浓硝酸具有氧化性,又说明了浓硝酸具有挥发性C.烧杯内氢氧化钠溶液的作用是除去尾气,防止尾气污染环境D.试管中浓硝酸可以用浓盐酸代替[导学号32390415]解析:选D
试管中浓硝酸易挥发,遇H2S气体,与之发生氧化还原反应生成单质S,A项和B项正确;烧杯中的NaOH溶液与逸出的酸性气体反应,防止污染环境,C项正确;浓盐酸无强氧化性,不能代替浓硝酸完成该实验,D项错误
3.下列实验方案正确且能达到相应实验目的的是()[导学号32390416]解析:选A
烧杯中的水冷却试管中的水蒸气,收集蒸馏水,A项正确;NO2可与水反应,不能用排水法收集,B项错;浓盐酸与二氧化锰反应制取氯气需要加热,C项错;D项中试管口应向下倾斜,D项错
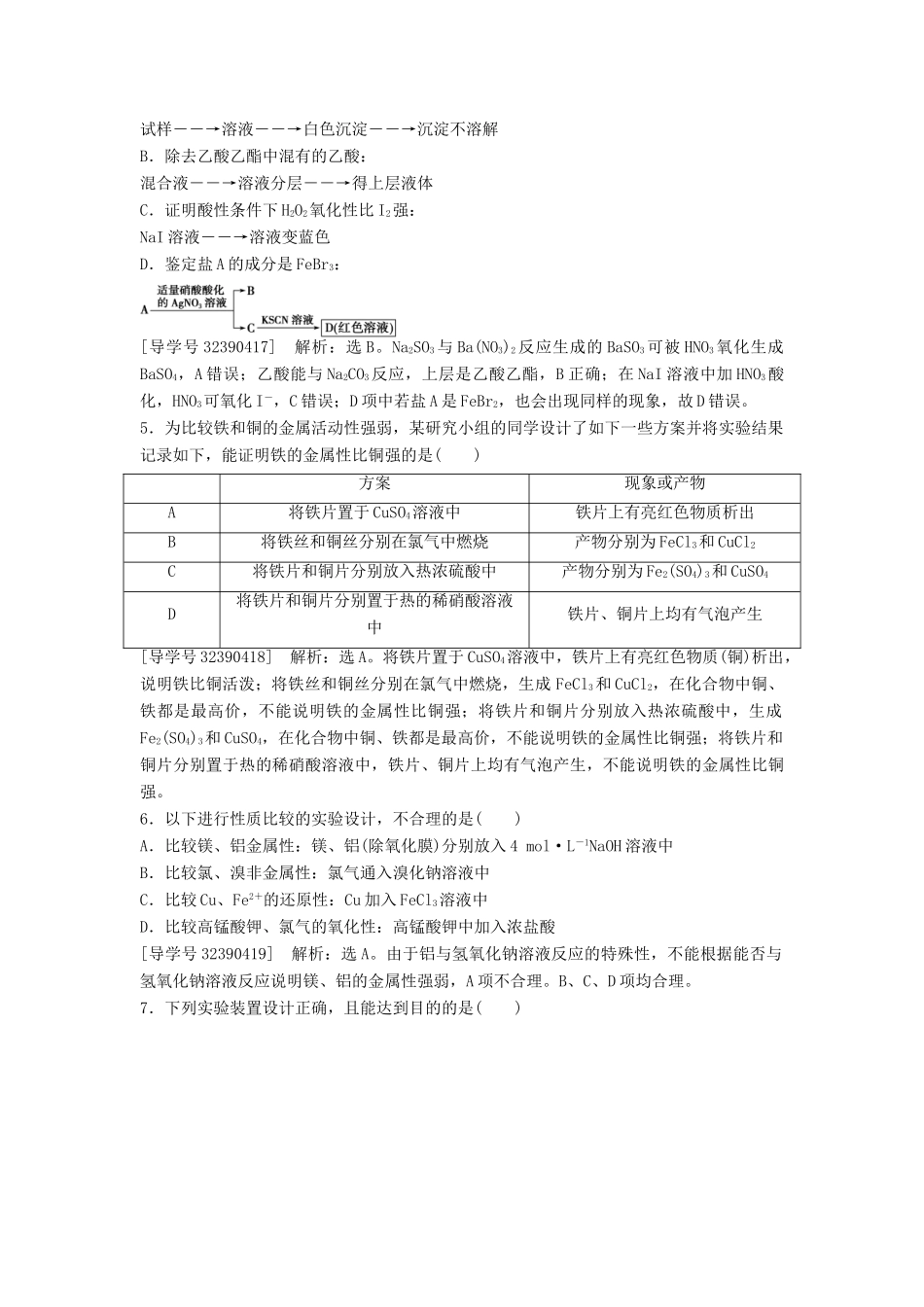
4.(2016·辽宁大连模拟)下列实验设计能够成功的是()A.检验亚硫酸钠试样是否变质:试样――→溶液――→白色沉淀――→沉淀不溶解B.除去乙酸乙酯中混有的乙酸:混合液――→溶液分层――→得上层液体C.证明酸性条件下H2O2氧化性比I2强:NaI溶液――→溶液变蓝色D.鉴定盐A的成分是FeBr3:[导学号32390417]解析:选B
Na2SO3与Ba(N