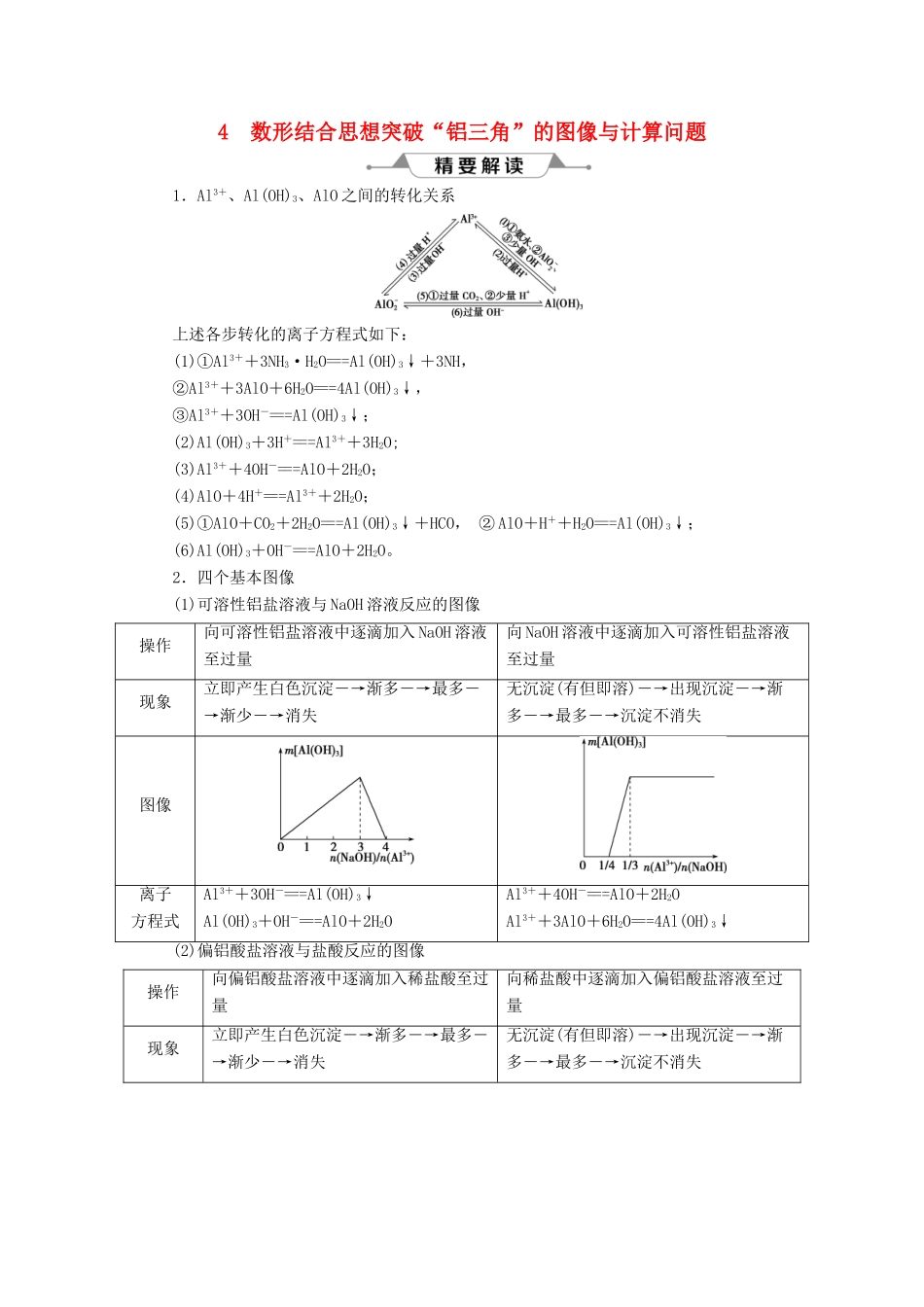
4数形结合思想突破“铝三角”的图像与计算问题1.Al3+、Al(OH)3、AlO之间的转化关系上述各步转化的离子方程式如下:(1)①Al3++3NH3·H2O===Al(OH)3↓+3NH,②Al3++3AlO+6H2O===4Al(OH)3↓,③Al3++3OH-===Al(OH)3↓;(2)Al(OH)3+3H+===Al3++3H2O;(3)Al3++4OH-===AlO+2H2O;(4)AlO+4H+===Al3++2H2O;(5)①AlO+CO2+2H2O===Al(OH)3↓+HCO,②AlO+H++H2O===Al(OH)3↓;(6)Al(OH)3+OH-===AlO+2H2O
2.四个基本图像(1)可溶性铝盐溶液与NaOH溶液反应的图像操作向可溶性铝盐溶液中逐滴加入NaOH溶液至过量向NaOH溶液中逐滴加入可溶性铝盐溶液至过量现象立即产生白色沉淀―→渐多―→最多―→渐少―→消失无沉淀(有但即溶)―→出现沉淀―→渐多―→最多―→沉淀不消失图像离子方程式Al3++3OH-===Al(OH)3↓Al(OH)3+OH-===AlO+2H2OAl3++4OH-===AlO+2H2OAl3++3AlO+6H2O===4Al(OH)3↓(2)偏铝酸盐溶液与盐酸反应的图像操作向偏铝酸盐溶液中逐滴加入稀盐酸至过量向稀盐酸中逐滴加入偏铝酸盐溶液至过量现象立即产生白色沉淀―→渐多―→最多―→渐少―→消失无沉淀(有但即溶)―→出现沉淀―→渐多―→最多―→沉淀不消失图像离子方程式AlO+H++H2O===Al(OH)3↓Al(OH)3+3H+===Al3++3H2OAlO+4H+===Al3++2H2OAl3++3AlO+6H2O===4Al(OH)3↓3
四个拓展图像(1)向AlCl3溶液中逐滴加入氨水或NaAlO2溶液至过量,图像如图1所示
(2)向NaAlO2溶液中逐滴加入Al