“实验室制取二氧化碳的探究”学案——化学实验探究课宜昌市九中班组组长组内成员探究时间一、课前准备(一)阅读下列信息,并填写下列空白
1、碳酸钠(Na2CO3)、大理石或石灰石[主要成分碳酸钙(CaCO3)]等碳酸盐,均能与稀盐酸(有效成分为HCl)[或稀硫酸(有效成分为H2SO4)]等酸直接反应生成二氧化碳;铜与稀盐酸(HCl)、稀硫酸(H2SO4)等酸不反应
2、二氧化碳的性质信息:(从生活经验和已有事实推测)(1)把燃烧的木条放入二氧化碳中,木条熄灭,说明
(2)打开汽水瓶盖可观察到,这个事实说明二氧化碳在水里的溶解性为:,且二氧化碳能与水反应
(3)向石灰水中吹气,现象为,说明二氧化碳能与石灰水中的氢氧化钙[Ca(OH)2]反应,以此来鉴定二氧化碳气体
(4)在标准状况下,二氧化碳的密度为1
977g/L,空气密度为1
293g/L
说明二氧化碳的密度比空气的密度
(5)由(2)和(4)可知,用法收集二氧化碳气体;由(1)可知验满方法为
(二)查找你所知道的能生成二氧化碳的反应,并从反应条件难易、原料是否易得、反应速度快慢、产生的气体是否便于收集等因素进行比较,思考这些反应能否用于实验室制取二氧化碳,什么原料是实验室制二氧化碳气体的理想原料
能生成二氧化碳的反应原料生成二氧化碳的化学反应方程式能否用于实验室制取二氧化碳的理由12345…二、活动与探究1、探究实验室制二氧化碳的理想原料
取三支试管,分别加入石灰石、碳酸钙粉末、碳酸钠粉末,分别向试管中加入稀硫酸;再取三支试管,分别加入石灰石、碳酸钙粉末、碳酸钠粉末,分别向试管中加入稀盐酸
观察现象,重点比较反应速度快慢,由此归纳实验室制二氧化碳气体的理想原料
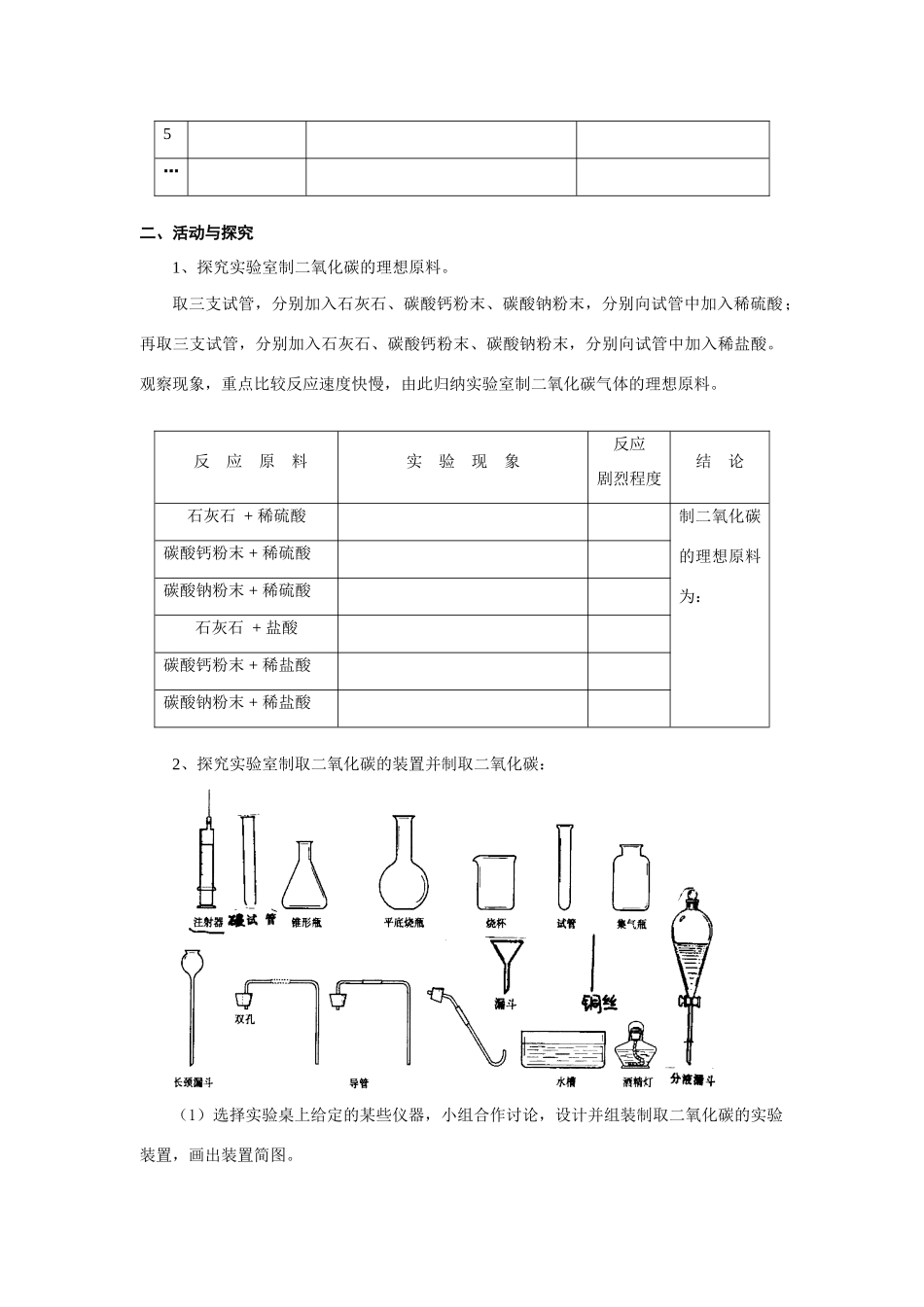
反应原料实验现象反应剧烈程度结论石灰石+稀硫酸制二氧化碳的理想原料为:碳酸钙粉末+稀硫酸碳酸钠粉末+稀硫酸石灰石+盐酸碳酸钙粉末+稀盐酸碳酸钠粉末+稀盐酸2、探究实