第6讲离子反应考纲要求1
了解电解质的概念
了解强电解质和弱电解质的概念
理解电解质在水溶液中的电离,以及电解质溶液的导电性
了解离子反应的概念、离子反应发生的条件
能正确书写离子方程式
考点一电解质及其电离1.电解质和非电解质(1)分类依据(2)电解质与物质类别的关系①酸、碱、盐全为电解质
②水和离子化合物型氧化物均为电解质
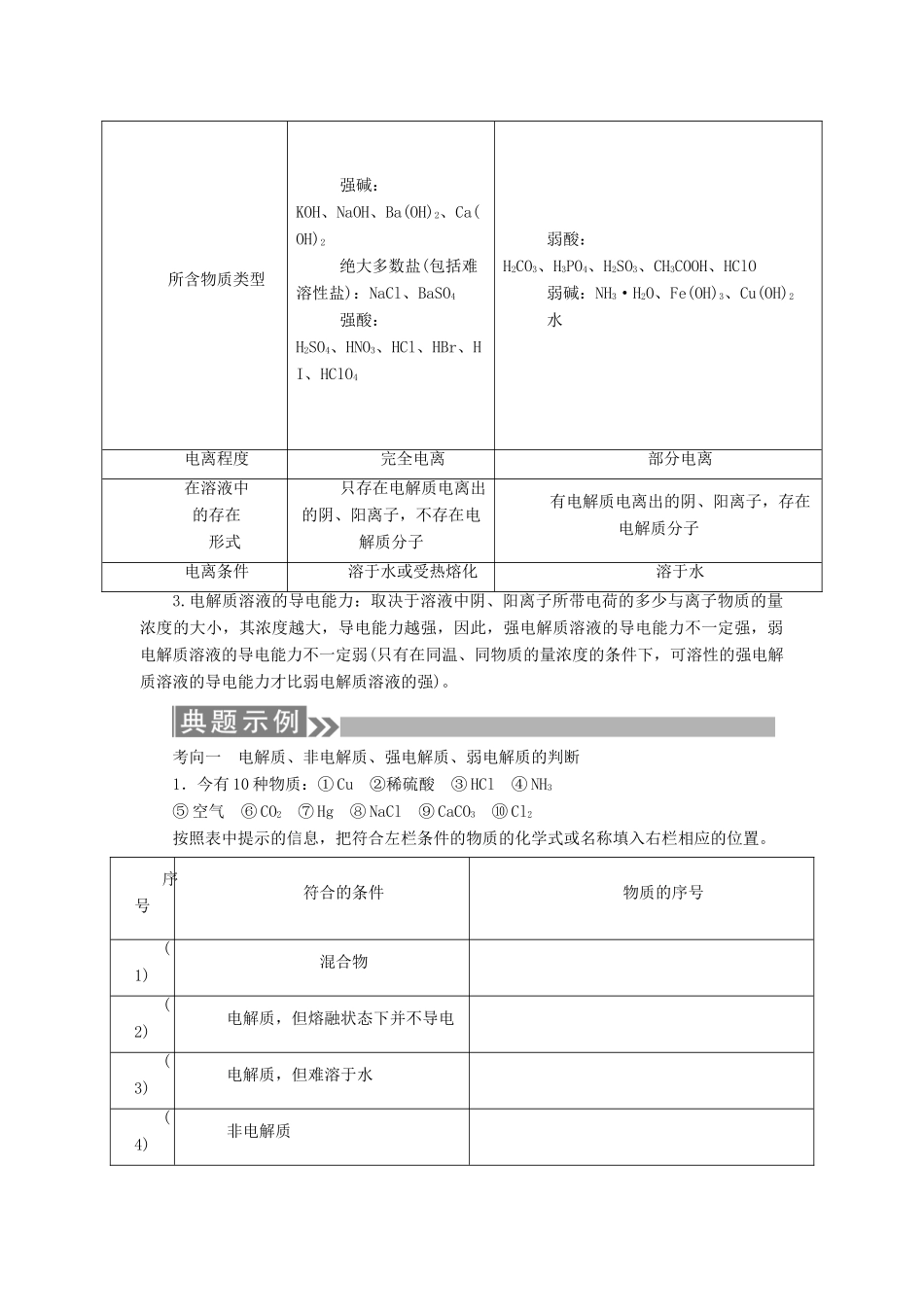
(3)电解质的强弱与物质类别的关系强电解质:强酸、强碱、绝大多数盐
弱电解质:弱酸、弱碱、少数盐(如醋酸铅)和水
2.电解质电离条件(1)共价化合物型电解质:溶于水
(2)离子化合物型电解质:溶于水或熔融
3.电离方程式的书写(1)强电解质的电离方程式中,用“===”连接,弱电解质(包括弱酸的酸式酸根)的电离方程式中,用“”连接
(2)多元弱酸的电离分步书写,多元弱碱的电离一步写完
如:H2CO3:H2CO3H++HCO,HCOH++CO;Fe(OH)3:Fe(OH)3Fe3++3OH-
(3)酸式盐的电离:多元强酸酸式盐与多元弱酸酸式盐的阴离子电离情况不同
如NaHSO4溶液中:NaHSO4===Na++H++SO;NaHCO3溶液中:NaHCO3===Na++HCO、HCOH++CO
【感悟测评】判断正误(正确的打“√”,错误的打“×”)
(1)银和食盐水都能导电,都属于电解质()(2)AgCl、BaSO4等不溶于水,都属于弱电解质()(3)强电解质溶液的导电能力比弱电解质溶液的导电能力强()(4)HClO是弱酸,但NaClO是强电解质()(5)在溶于水或熔融状态下能够自身发生电离的化合物一定是电解质()(6)强电解质都是离子化合物,弱电解质都是共价化合物()(7)SO2溶于水可导电,故SO2属于电解质()答案:(1)×(2)×(3)×(4)√(5)√(6)×(7)×【多维思考】1.(RJ必修1·P33,3改编)下列状态的物质,既能导