课时3物质的性质探究化学反应条件的控制[考纲导航]知识条目必考要求选考要求选考分布2015201620179月10月4月10月4月(1)铝片(条)燃烧的方法b(2)铝表面氧化膜的作用b(3)观察有机物颜色和状态及辨别有机物气味的方法a(4)用乙醇和浓硫酸制取乙烯的原理、方法和操作b(5)乙醇、苯酚分子中羟基的化学活性比较b(6)盐酸、碳酸、苯酚酸性比较b(7)硫代硫酸钠和强酸反应的原理及现象b(8)浓度、温度对硫代硫酸钠与酸反应速率的影响b(9)不同的催化剂对同一反应的催化效果c(10)变量控制在实验研究中的应用c31(4)31(3)(11)氯化钴溶液的变色原理b(12)浓度、温度变化对氯化钴溶液平衡体系的影响b(13)不同条件下(酸、碱性)乙酸乙酯水解的速率和程度b考点一物质的性质探究[主干精讲]1
化学实验的过程探究2
铝及其化合物性质的实验探究实验探究项目实验方案设计现象、解释及问题铝与氧气反应将铝片剪成长5~8cm,宽0
3cm铝条,绕成螺旋状,一端缠绕一根火柴,坩埚钳夹住铝条另一端,点燃铝条上的火柴,待火柴快燃烧完时,将铝条伸入装有O2的集气瓶中(瓶内盛少量水),观察现象实验现象:剧烈燃烧、发出耀眼的白光方程式:4Al+3O2=====2Al2O3结论:通过去保护膜,增加氧气的浓度增大铝的接触面积等使铝在氧气中燃烧铝表面氧化膜的实验探究1
取3片铝片,将其中两片铝片用砂纸擦去表面的氧化膜破坏铝表面氧化膜的方法:①用砂纸擦;②用NaOH溶液;③用稀酸浸泡2
将一片擦去氧化膜的铝片放入20mL0
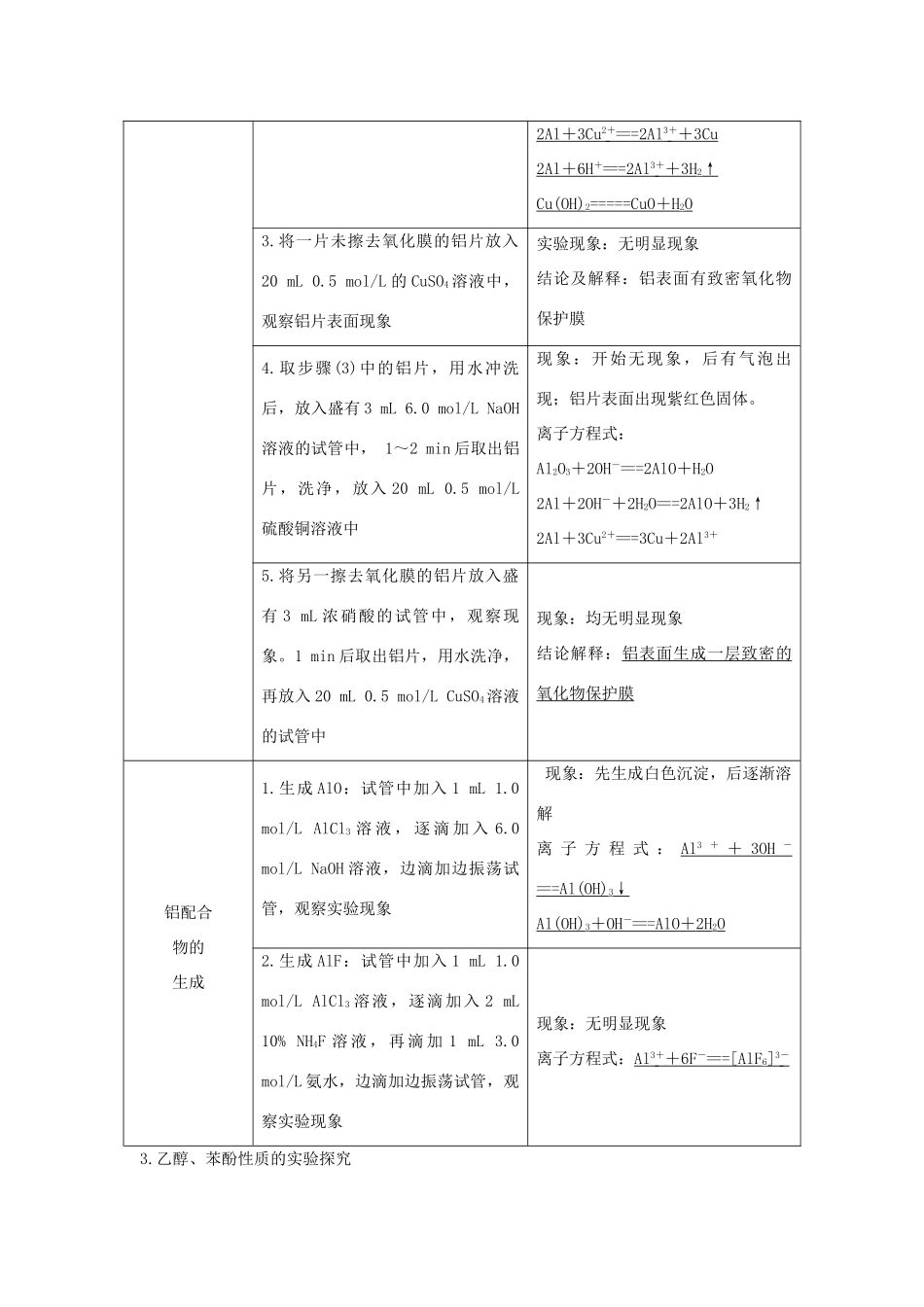
5mol/L的CuSO4溶液中,观察铝片表面现象及其他可能发生的现象实验现象:铝表面有红色物质出现同时有少量气泡,铝片上下翻滚,溶液中出现黑色物质
化学方程式:Cu2++2H2OCu(OH)2+2H+2Al+3Cu2+===2Al3++3Cu2Al+6H+===2Al