第26讲弱电解质的电离平衡考纲要求1
理解强电解质和弱电解质的概念
了解电解质在水溶液中的电离以及电解质溶液的导电性
理解弱电解质在水溶液中的电离平衡
考点一弱电解质的电离平衡1.强、弱电解质(1)定义与物质类别(2)电离方程式的书写——“强等号,弱可逆,多元弱酸分步离”①强电解质:如H2SO4:H2SO4===2H++SO
②弱电解质:a.一元弱酸,如CH3COOH:CH3COOHCH3COO-+H+
b.多元弱酸,分步电离,分步书写且第一步电离程度远远大于第二步的电离程度,如H2CO3:H2CO3H++HCO、HCOH++CO
c.多元弱碱,分步电离,一步书写
如Fe(OH)3:Fe(OH)3Fe3++3OH-
③酸式盐:a.强酸的酸式盐如NaHSO4在水溶液中:NaHSO4===Na++H++SO;熔融时:NaHSO4===Na++HSO
b.弱酸的酸式盐:“强中有弱”,如NaHCO3:NaHCO3===Na++HCO、HCOH++CO
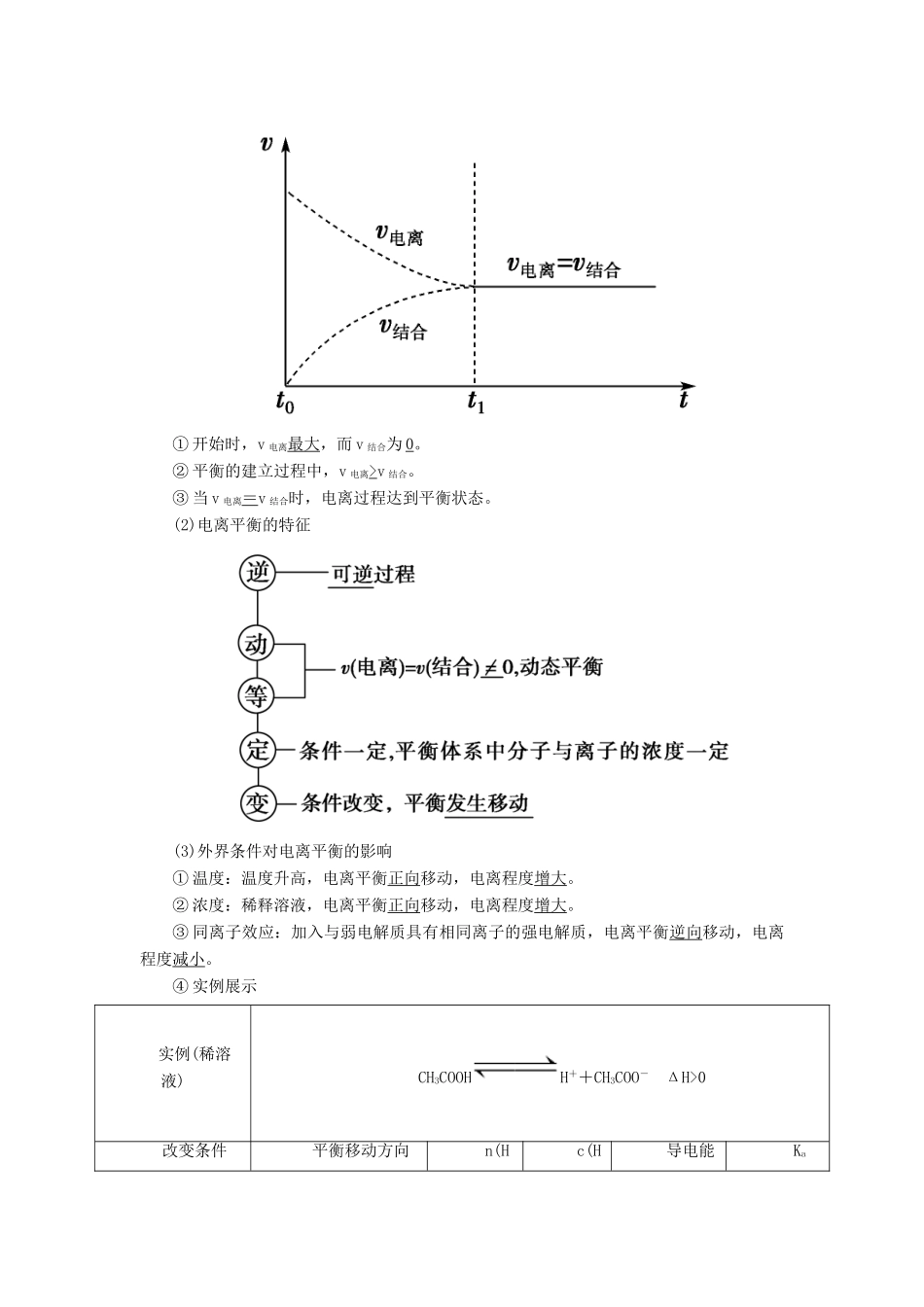
2.弱电解质的电离平衡(1)电离平衡的建立①开始时,v电离最大,而v结合为0
②平衡的建立过程中,v电离>v结合
③当v电离=v结合时,电离过程达到平衡状态
(2)电离平衡的特征(3)外界条件对电离平衡的影响①温度:温度升高,电离平衡正向移动,电离程度增大
②浓度:稀释溶液,电离平衡正向移动,电离程度增大
③同离子效应:加入与弱电解质具有相同离子的强电解质,电离平衡逆向移动,电离程度减小
④实例展示实例(稀溶液)CH3COOHH++CH3COO-ΔH>0改变条件平衡移动方向n(Hc(H导电能Ka+)+)力加水稀释→增大减小减弱不变加入少量冰醋酸→增大增大增强不变通入HCl(g)←增大增大增强不变加NaOH(s)→减小减小增强不变加入镁粉→减小减小增强不变升高温度→增大增大增强增大加CH3COONa(s)←减小减小增强不变【