12016年东北三省四市教研联合体高考化学一模试卷一、选择题:本题共7小题,每小题6分,在每小题给出的四个选项中,只有一项是符合题目要求的.1.化学与人类社会的生产、生活有着密切联系.下列叙述中正确的是()A.铜制品既能发生吸氧腐蚀又能发生析氢腐蚀B.铝制品由于表面有致密的氧化膜,可以稳定存在于空气中C.苹果放在空气中久置变黄和漂白过纸张久置变黄原理相似D.高纯度的SiO2对光有很好的折射和全反射作用,可以制成光电池将光能直接转化为电能2.青蒿素是抗疟特效药属于萜类化合物,如图所示有机物也属于萜类化合物,该有机物的一氯取代物有(不含立体异构)()A.5种B.6种C.7种D.8种3.下列离子方程式正确的是()A.金属钠与水反应:Na+H2O═Na++H2B.氯化铵溶液显酸性的原因:NH4++H2O═NH3
H2O+H+C.AICl3溶液中加入足量氨水:Al3++4NH3
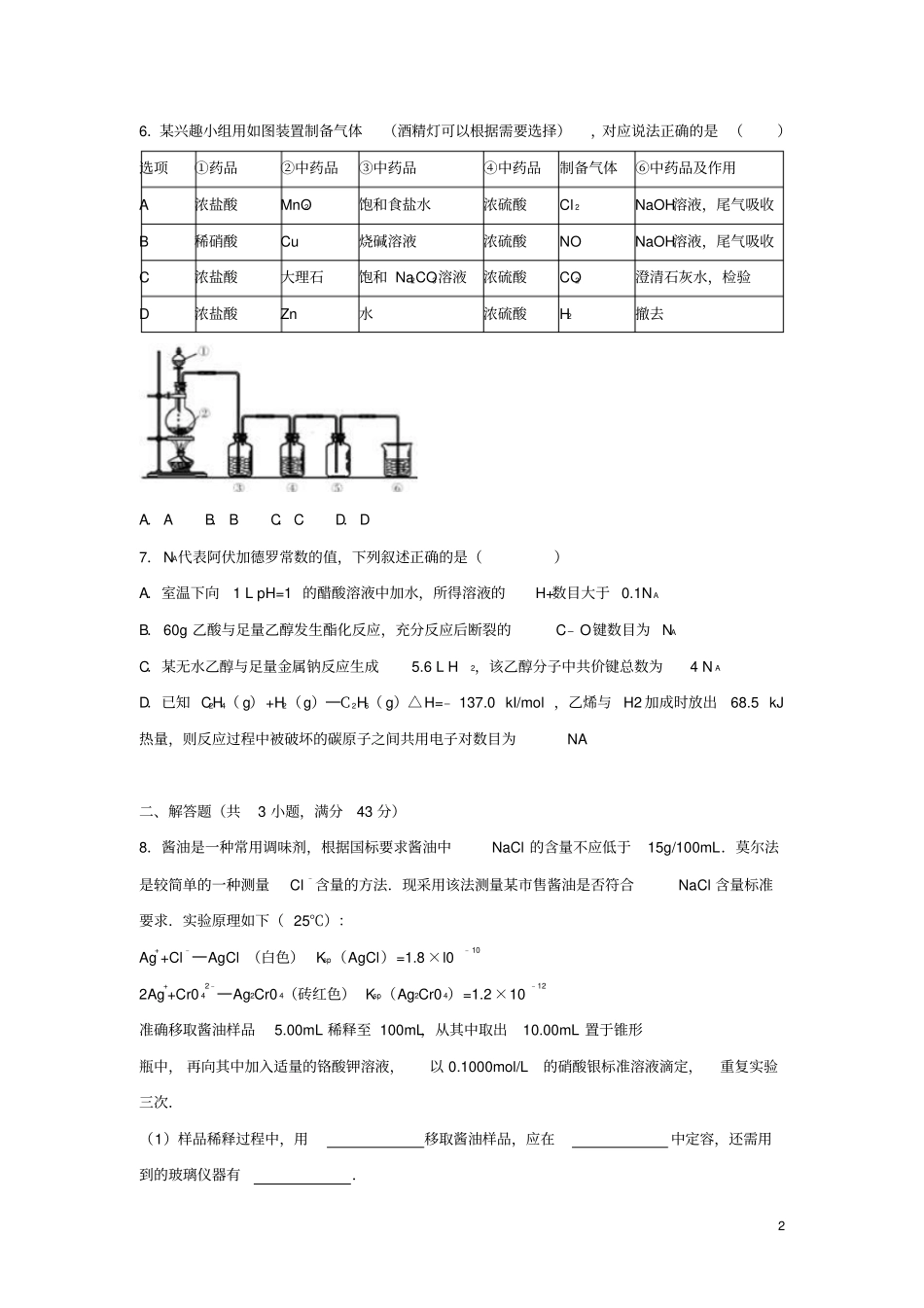
H2O═AlO2﹣+4NH4+2H2OD.氯化铁溶液中滴加少量的硫化氢溶液:2Fe3++H2S═2Fe2++S+2H+4.丙烯酸的结构简式为CH2=CH﹣COOH,下列关于丙烯酸的说法错误的是()A.丙烯酸可以发生取代反应B.丙烯酸可以使酸性高锰酸钾溶液褪色C.丙烯酸与HBr发生加成反应只能得到唯一产物D.丙烯酸钠溶液中Na+浓度大于丙烯酸根离子浓度5.X、Y、Z、R、W是5种短周期元素,原子序数依次增大,它们可组成离子化合物Z2Y和共价化合物RY3、XW4,已知Y、R同主族,Z、R、W同周期.下列说法不正确的是()A.原子半径:Z>R>WB.X2W6分子中各原子均满足8电子结构C.气态氢化物沸点:HmY>HnRD.Y、Z、R三种元素组成的化合物水溶液一定显碱性26.某兴趣小组用如图装置制备气体(酒精灯可以根据需要选择),对应说法正确的是()选项①药品②中药品③中药品④中药品制备气体⑥中药品及作用A浓盐酸Mn