1/5化学学习中的顺口溜记忆法元素周期表的结构:(记忆口诀)七横十八纵,三短加三长,第七尚未满,有待我们装;七主分两边,七副中间站,零族排末尾,八族括三纵;镧锕单独列,每系占一格
第一周期:氢氦第二周期:锂铍硼碳氮氧氟氖第三周期:钠镁铝硅磷硫氯氩第四周期:钾钙钪钛钒铬锰铁钴镍铜锌镓锗砷硒溴氪第五周期:铷锶钇锆铌钼锝钌铑钯银镉铟锡锑碲碘氙第六周期:铯钡镧铪钽钨铼锇铱铂金汞铊铅铋钋砹氡第七周期:钫镭锕最外层电子数=主族序数=最高正化合价第一周期:HHe第二周期:LIBeBCNOFNe第三周期:NaMgAlSiPSClAr第四周期:KCaScTiVCrMnFeCoNiCuZnGaGeAsSeBrKr第五周期:RbSrYZrNbMoTeRuRhPdAgCdInSnSbTeIXe第六周期:CsBaLaHfTaWReOsIrPtAuHgTlPbBiPoAtRn第七周期:FrRaAc注:黄色字——气态;蓝色字——液态;红色字——金属;绿色字——非金属氢氦锂铍硼,碳氮氧氟氖;钠镁铝硅磷,硫氯氩钾钙;钪钛钒铬锰,铁钴镍铜锌;镓锗砷硒溴,氪铷锶钇锆;铌钼锝钌铑,钯银镉铟锡;锑碲碘氙铯,钡镧铪钽钨;2/5铼锇铱铂金,汞铊铅铋钋;砹氡钫镭锕,A
同一周期中元素性质的递变规律(以第三周期为例:)*最外层电子数由1个递增到8个*元素的金属性逐渐减弱,非金属性逐渐增强*最高氧化物及其对应的水化物的碱性逐渐减弱,酸性逐渐增强*元素的最高正化合价由+1逐渐增加到+7,而负化合价从第四主族开始,由-4增加到-1,最后一种元素最外层电子数为8,是稀有气体,化合价为0*元素的原子半径逐渐缩小
同一主族元素性质的递变规律同一主族元素自上而下,由于电子层数增加,原子半径增大,核对外层电子的吸引力减小,失去电子的能力增大,则元素的金属性依次增强,而非金属性依次减弱
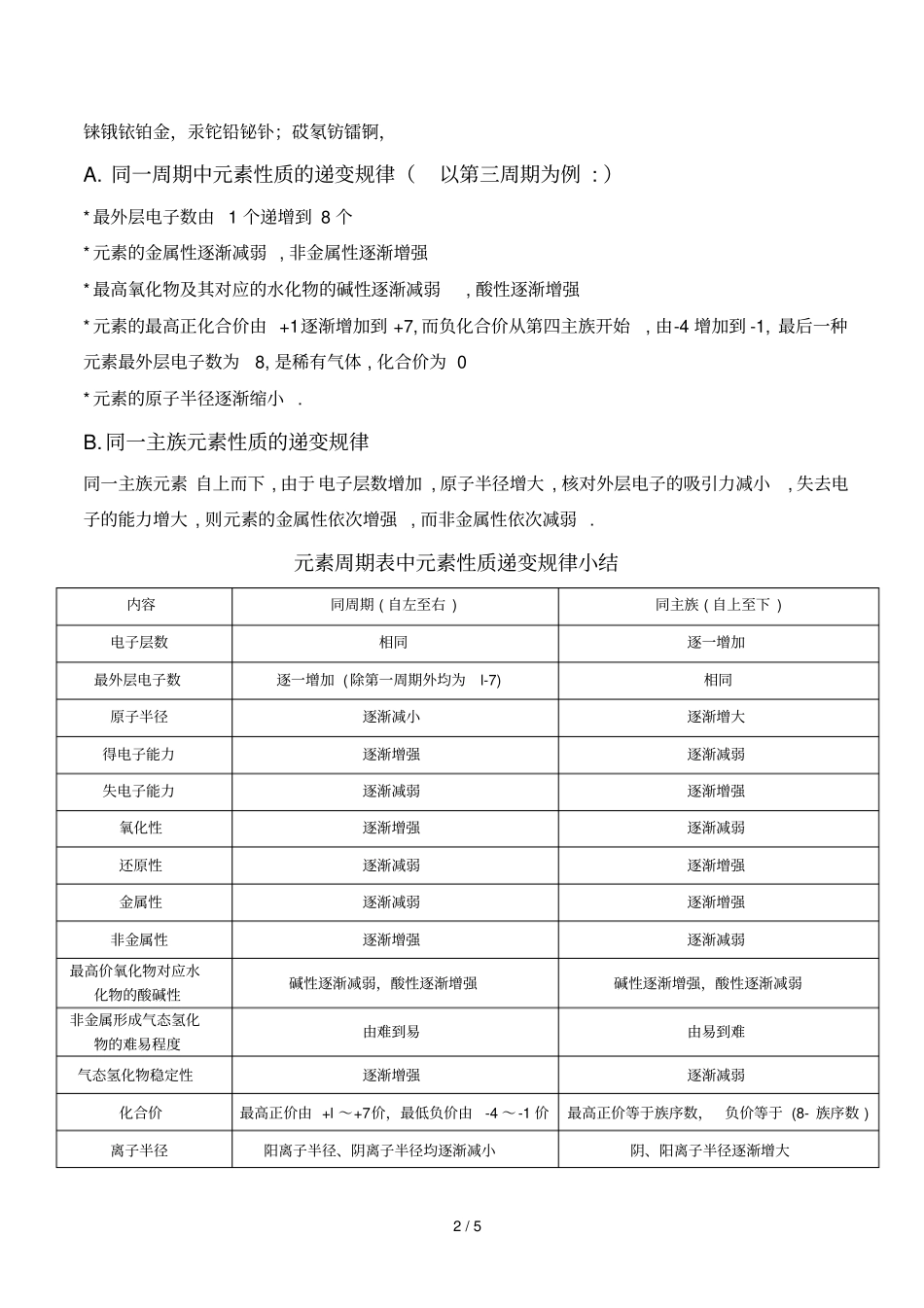
元素周期表中元素性质递变规律小结内容同周期(自左至