微项目海带提碘与海水提溴--体验元素性质递变规律的实际应用新知预习1
卤族元素化学性质的递变规律(F-I)(1)相似性
卤素原子最外层电子数都为7,都能形成气态氢化物(通式为HX),最高价氧化物对应的水化物化学式为HXO(F除外),单质具有氧化性
4(2)递变性
①单质氧化性逐渐减弱
②卤素离子还原性逐渐增强
③气态氢化物稳定性逐渐减弱
④单质与氢气反应的能力逐渐减弱
(3)溴、碘单质物理性质比较性质Br2I2颜色深红棕色紫黑色状态液体固体溶解性水中溶解度不大溶解度不大有机溶剂中易溶易溶特性易挥发、有毒①易升华②使淀粉变蓝2
卤素单质的氧化性:F>Cl>Br>1
萃取与分液(1)萃取原理
利用某溶质在两种互不相溶的溶剂里溶解能力的不同,用一种溶剂(萃取剂)将其从原溶剂中提取出来的方法叫作萃取
将萃取后两种互不相溶的液体分开的操作,叫作分液
(2)实验步骤
加萃取剂(如图I)——振荡萃取(如图II)——静置分层(如图III)——分液(如图W):微思考2】灼烧海带时用到哪些仪器
圈£4灼烧海芾项目活动一1
从海带中提取碘问题探究(1)海带中的碘元素主要以I-的形式存在,提取时用适当的氧化剂将其氧化成12,再萃取出来
可用什么氧化剂
makepdikM澳水和〔:0|的渥命物(】)加苓取郝⑵監藹萃血时)恭最外恳外液4
分离和提纯的一般方法(1)物理方法:过滤、蒸发结晶、蒸馏或分馏、萃取、分液、升华等
(2)化学方法:沉淀法、洗气法、转化法等
海水提溴从海水中提取溴,一般要经历浓缩、氧化和提取三个步骤
在海水提溴的化工生产中,常选用氯气作为氧化剂,反应原理为Cl2+2Br-=2Cl-+Br2
【微思考1】可否用酒精萃取溴水中的溴
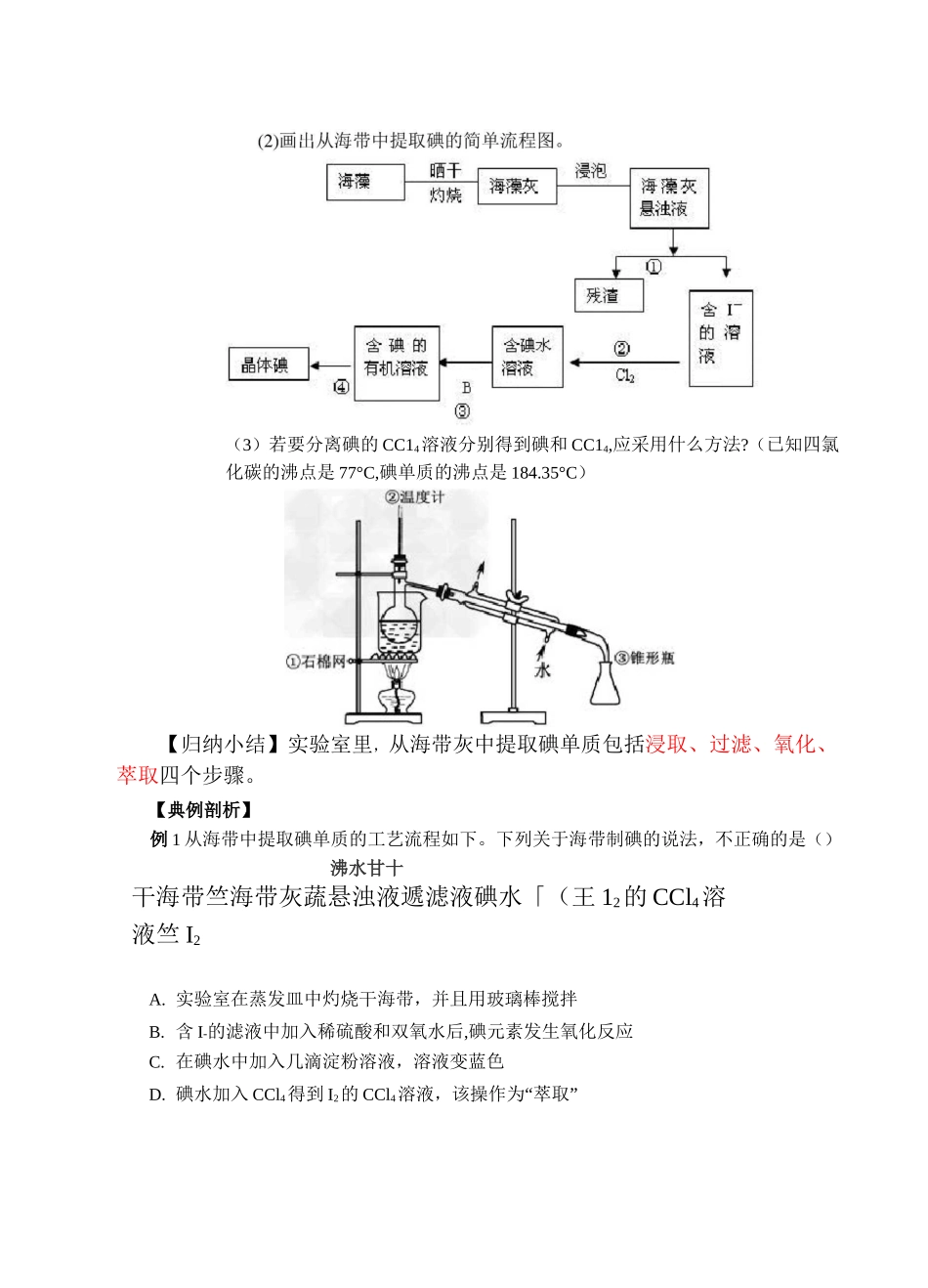
(3)若要分离碘的CC14溶液分别得到碘和CC14,应采用什么方法
(已知四氯化碳的沸点是77°C,碘单质的沸点是184