用重铬酸钾电位滴定硫酸亚铁铵溶液实验目的:学习氧化还原滴定法的原理与实验方法,各种滴定终点确定方法(V~E曲线法,二次微商法)
实验原理:用K2Cr2O7滴定Fe2+,其反应式如下:K2Cr2O7+6Fe2++14H+→2Cr3++6Fe3++H2O利用铂电极作指示电极,饱和甘汞电极作参比电极,与被测溶液组成工作电池
在滴定过程中,随着滴定剂的加入,铂电极的电极电位发生变化
在化学计量点附近铂电极的电极电位产生突跃,从而确定滴定终点
仪器和试剂:仪器:饱和甘汞电极铂电极pH—mv计滴定管(酸式)搅拌磁试剂:K2Cr2O7溶液(0
01mol/L)硫酸亚铁铵溶液二苯胺磺酸钠(指示剂)实验步骤:1.准备好铂电极和饱和甘汞电极;在滴定管中加入重铬酸钾标准滴定溶液
2.试样的配制:在50mL烧杯中,将10mLFe2+和8mL3mol的H2SO4相混合;再加入几滴二苯胺磺酸钠作指示剂
3.用酸式滴定管装入0
01mol/L:K2Cr2O7溶液,排气泡,调零后置于铁架台上4.试液中Fe2+含量的测定:开动搅拌磁子,待电位值稳定后读数
向烧杯中滴加K2Cr2O7溶液,记录滴定剂为1mL,2mL,3mL,4mL,4
0mL处的电动势值
5.关闭仪器和搅拌电源开关
清洗滴定管,电极,烧杯并放回原处
6.根据数据,给出E-V曲线,确定滴定终点;用二次微商法确定终点,比较两种结果
实验现象:溶液因加入了指示剂,随着K2Cr2O7溶液的加入,溶液由无色变成浅绿色最后变成紫色,可帮助指示滴定终点
当K2Cr2O7溶液加入的体积达到4
8mL时,电位发生突跃
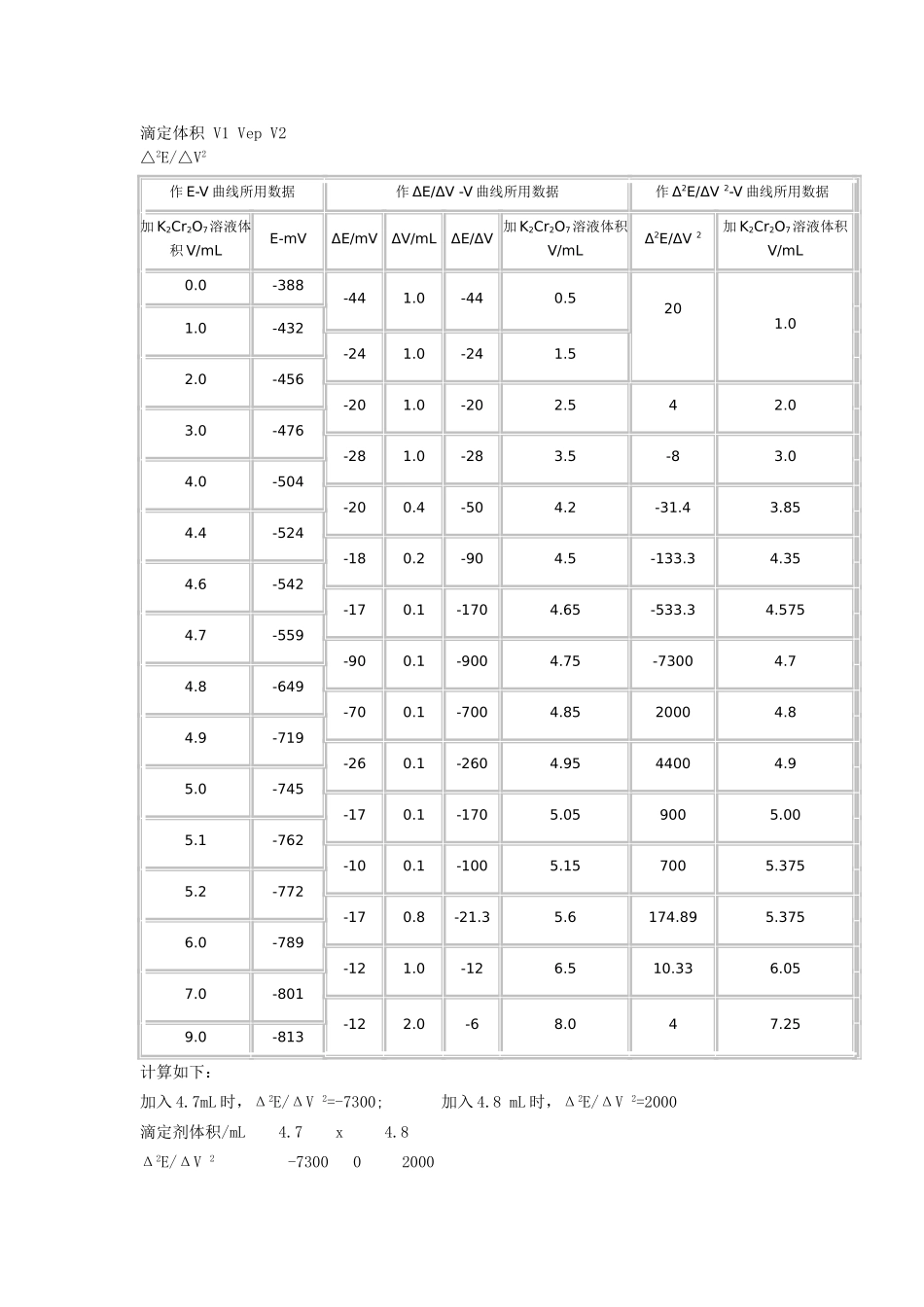
实验结果:1.实验数据记录如下:V(K2Cr2O7)(mL)0