第二章电解质溶液学案强电解质和弱电解质目的要求:1.从电解质电离程度掌握强电解质和弱电解质
2.认识弱电解质存在电离平衡
3.认识有弱电解质生成的离子互换反应能发生的原理
4.认识弱电解质在离子反应过程中电离平衡能够发生移动
教学重点:电离平衡及平衡移动教学难点:电离平衡及平衡移动教学过程:引入1.氯化钠晶体、溶液、熔融的导电事实2.电流产生的原因(电动势、自由移动的电荷新课电解质导电是因为他的水溶液或熔化状态能产生自由移动的离子,但是,不同的电解质在水溶液中的导电能力是否相同呢
演示实验2-1(P28)现象:分析(1)灯亮,导电,有自由移动的离子存在(2)灯有明有暗:说明自由离子的浓度不同(3)相同浓度、体积的不同电解质,为什么溶液中自由离子的浓度不同板书第一节强电解质和弱电解质一.电解质(1)概念:凡是在水溶液里或熔化状态下能够导电的化合物(酸、碱、盐)
(2)电离:NaCl=Na++Cl-NaOH=Na++OH-H2SO4=2H++SO42-HCl=H++Cl-设问是否所有的电解质都能在水溶液中全部电离成相应的离子呢
或者说不同的电解质在其水溶液中导电能力是否相同
我们一起再来观察实验现象
演示实验2——1强调:5种溶液的浓度均相同、体积相同、电压相同、电极踞相同等,此时灯的亮度与什么因素有关
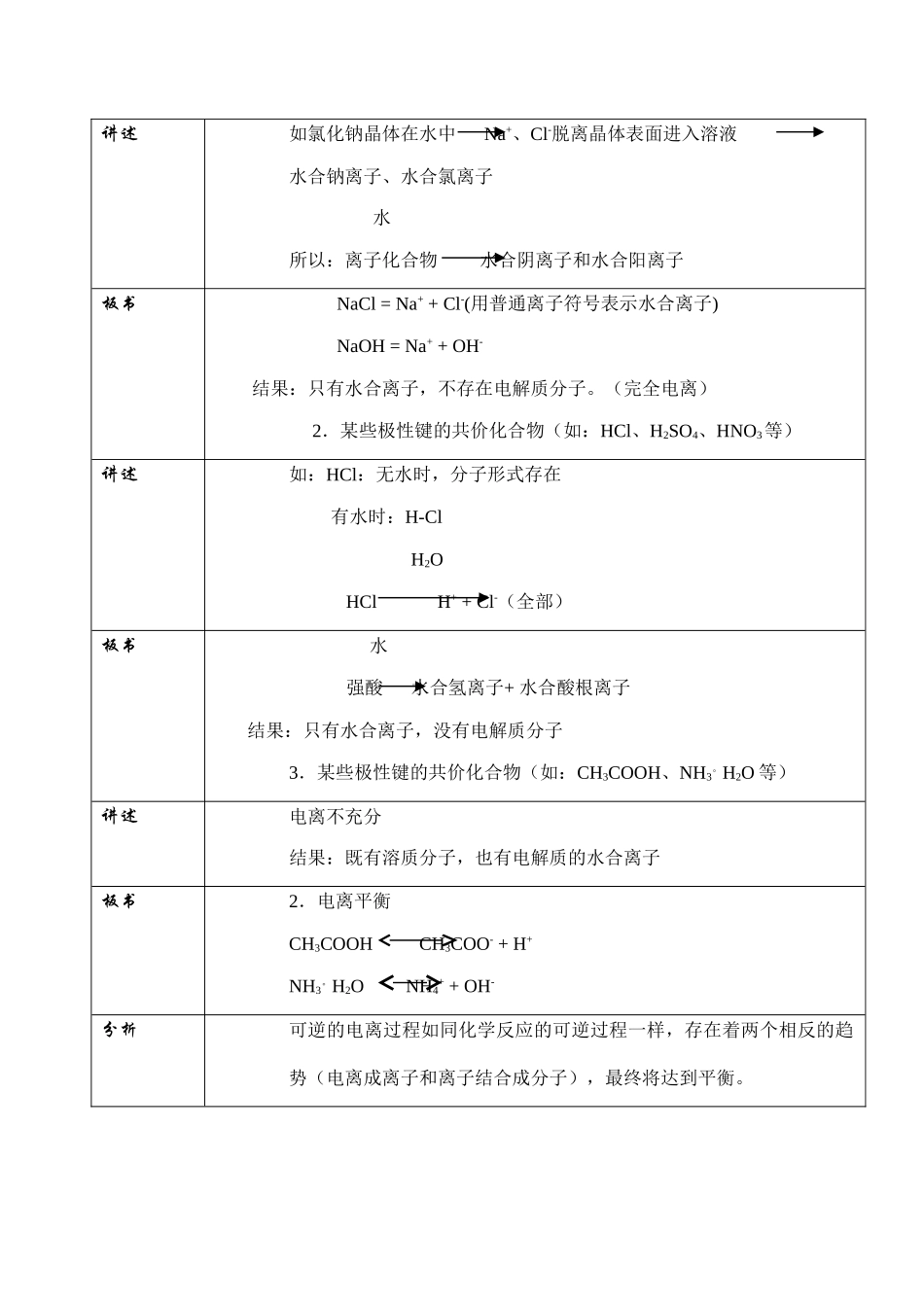
实验现象:灯亮:盐酸、氢氧化钠、氯化钠灯暗:氨水、醋酸结论亮暗导电性:强弱离子浓度:大小电离程度:完全不完全电解质分类:强电解质弱电解质板书二.强电解质和弱电解质1.不同电解质在水溶液中的存在形式离子化合物(如:盐类、强碱)讲述如氯化钠晶体在水中Na+、Cl-脱离晶体表面进入溶液水合钠离子、水合氯离子水所以:离子化合物水合阴离子和水合阳离子板书NaCl=Na++Cl-(用普通离子符号表示水合离子)NaOH=Na++OH-结果:只有水合离子,不存在电解质分子
(完全电离)2.某些